题目内容
 如图所示,用排饱和食盐水法先后收集20ml CH4和80ml Cl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题:
如图所示,用排饱和食盐水法先后收集20ml CH4和80ml Cl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题:(1)大约30min后,可以观察到量筒壁上出现
油状
油状
状液体,该现象说明生成了②③④
②③④
(填序号)①CH3Cl; ②CH2Cl2;③CHCl3; ④CCl4量筒内出现的白雾是盐酸的小液滴
盐酸的小液滴
,量筒内液面上升
上升
(填“上升”、“下降”或“不变”),(2)使0.5摩尔甲烷和氯气发生取代反应,生成相同物质的量的四种有机取代物,则需要氯气的物质的量是
C
C
A.2.5mol;B.2mol;C.1.25mol; D.0.5mol(3)液化石油气的主要成分是丙烷,试写出丙烷燃烧的化学方程式
C3H8+5O2
3CO2+4H20
| ||
C3H8+5O2
3CO2+4H20
.将现用液化石油气的燃具改用天然气时应
| ||
减少
减少
进空气的风口.(填增大或减少)(4)下列烷烃的分子式有 3种同分异构体的是
A
A
.(填字母)A.C5H12;B.C4H10; C.C3H8;D.C2H6.分析:(1)二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,的氯化氢极易溶于水,遇水蒸气形成白雾,容器中的压强较低,液面上升;
(2)四种取代物的物质的量相同,即各为0.125mol,发生取代反应时,一半的Cl进入HCl;
(3)丙烷燃烧生成二氧化碳和水;
(4)烷烃同分异构体书写技巧:先写最长链;然后从最长链减少一个碳原子作为取代基,在剩余的碳链上连接,即主链由长到短,支链由整到散,位置由中心排向两边.
(2)四种取代物的物质的量相同,即各为0.125mol,发生取代反应时,一半的Cl进入HCl;
(3)丙烷燃烧生成二氧化碳和水;
(4)烷烃同分异构体书写技巧:先写最长链;然后从最长链减少一个碳原子作为取代基,在剩余的碳链上连接,即主链由长到短,支链由整到散,位置由中心排向两边.
解答:解:(1)甲烷可以和氯气发生取代反应,生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,一氯甲烷是气体,生成的氯化氢极易溶于水,遇水蒸气形成白雾,容器中的压强较低,液面上升,故答案为:油状;②③④;盐酸的小液滴;上升;
(2)四种取代物的物质的量相同,即各为0.125mol,发生取代反应时,一半的Cl进入HCl,消耗氯气的物质的量为0.125mol+2×0.125mol+3×0.125mol+4×0.125mol=1.25mol,故选C;
(3)丙烷燃烧生成二氧化碳和水,同体积的两种燃气,液化石油气耗氧量多,把液化石油气的灶具改用天然气为燃料时,需要减少空气气的量,故答案为:C3H8+5O2
3CO2+4H20;减少;
(4)C5H123种同分异构体;C4H102种同分异构体;C3H8、C2H6无同分异构体,故选A.
(2)四种取代物的物质的量相同,即各为0.125mol,发生取代反应时,一半的Cl进入HCl,消耗氯气的物质的量为0.125mol+2×0.125mol+3×0.125mol+4×0.125mol=1.25mol,故选C;
(3)丙烷燃烧生成二氧化碳和水,同体积的两种燃气,液化石油气耗氧量多,把液化石油气的灶具改用天然气为燃料时,需要减少空气气的量,故答案为:C3H8+5O2
| ||
(4)C5H123种同分异构体;C4H102种同分异构体;C3H8、C2H6无同分异构体,故选A.
点评:本题考查甲烷与氯气的燃烧、同分异构体书写,难度较小,旨在考查学生对基础知识的理解与掌握.

练习册系列答案
相关题目
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。
请填写下列空白: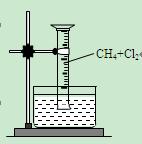
【实验一】用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
(1)该反应的化学方程式为 ▲ ;(只写第一步)
(2)水槽中盛放的液体最好为 ▲ ;(填标号)
| A.水 | B.饱和石灰水 | C.饱和食盐水 | D.饱和NaHCO3溶液 |
(3)该实验设计的错误之处 ▲ ;
【实验三】
步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL 蒸馏水,充分振荡,测得pH = 1.00。
(4)判断该反应中有氯化氢生成的依据是 ▲ ;
(5)假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00 mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为 ▲ mL;
(10分)某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
[实验一]用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
(1)该反应的化学方程式为 ;(只写第二步)
(2)水槽中盛放的液体最好为 ;(填标号)
| A.水 | B.饱和石灰水 | C.饱和食盐水 | D.饱和NaHCO3溶液 |
滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(3)该实验设计的错误之处 ;
[实验三]
步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL 蒸馏水,充分振荡,测得pH = 1.00。
(4)判断该反应中有氯化氢生成的依据是 ;
(5)假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00 mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为 mL;
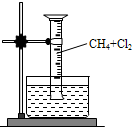 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.