题目内容
6.由CH3-CH2Cl为原料制取HOCH2-CH2OH,最好选取的反应类型是( )| A. | 消去、加成、取代 | B. | 加成、取代、水解 | C. | 取代、加成、消去 | D. | 加成、取代、消去 |
分析 由CH3-CH2Cl为原料制取HOCH2-CH2OH,需要卤代烃先反应生成烯烃,然后烯烃再转化为1,2-二卤代物,1,2-二卤代物再转化为乙二醇.
解答 解:由CH3-CH2Cl为原料制取HOCH2-CH2OH,需要卤代烃先反应生成烯烃,然后烯烃再转化为1,2-二卤代物,1,2-二卤代物再转化为乙二醇,所以一氯乙烷先发生消去反应生成乙烯,乙烯和溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷再发生水解反应或取代反应生成乙二醇,所以反应类型先后顺序是:消去、加成、取代,故选A.
点评 本题考查有机物合成,侧重考查学生合成路线设计能力,明确官能团及其性质、常见有机反应类型的关系是解本题关键,需要学生有综合运用知识能力,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
17.常温下,下列各溶液的叙述中正确的是( )
| A. | pH=7的NaHSO3与Na2SO3混合溶液中:c(Na+)=c(HSO3-)+c(SO32-) | |
| B. | 等物质的量浓度的下列溶液中:①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4 ④NH3•H2O,c(NH4+)由大到小的顺序是①>②>③>④ | |
| C. | 0.1 mol•L-1的醋酸的pH=a,0.01 mol•L-1的醋酸的pH=b,则a+1=b | |
| D. | 0.1 mol•L-1的醋酸钠溶液20 mL与0.1 mol•L-1的盐酸10 mL混合后溶液显酸性,则有:c(CH3COOH)>c(H+)>c(Cl-)>c(CH3COO-) |
1.反应4NH3(g)+5O2(g)$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O在2L的密闭容器中进行,30s后NO的物质的量增加了0.30mol.下列说法正确的是( )
| A. | 容器中NH3的物质的量一定增加了0.30mol | |
| B. | 容器中H2O(g)的物质的量至少为0.45mol | |
| C. | NH3的平均反应速率为0.010mol/(L•s) | |
| D. | NH3、O2、NO、H2O的物质的量之比一定为4:5:4:6 |
11.甲苯的两个氢原子分别被羟基和氯原子取代,则可形成的有机物同分异构体有( )
| A. | 10种 | B. | 16种 | C. | 17种 | D. | 20种 |
15.下列各项中两个反应不属于同一反应类型的是( )
| A. | 由苯与氢气生成环己烷;由乙烯制一氯乙烷 | |
| B. | 乙醇与乙酸制取乙酸乙酯;油脂的皂化反应 | |
| C. | 乙烯与氧气制环氧乙烷;乙醇制乙醛 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色;丙烯酸使溴水褪色 |
16.用如图1所示装置分别进行实验,请回答下列问题:

(1)导管E的作用是:保持锥形瓶和分液漏斗间的压强恒定,使液体能顺利滴下、消除因液体的滴入引起的体积误差;
(2)实验I烧瓶B中发生反应的化学方程式是CaC2+2H2O→Ca(OH)2+C2H2↑,产生的气体经验纯后点燃,现象是火焰明亮并伴有浓烈的黑烟;
(3)实验Ⅱ剩余的NH3需吸收处理.以下各种尾气吸收装置中如图2,不能防止倒吸的是be;
(4)实验Ⅲ的实验目的是验证生铁在潮湿空气中会发生吸氧腐蚀.则A中试剂可选用ac(填序号);
a.NaOH溶液 b.C2H5OH c.NaCl溶液 d.稀硫酸
能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是C管的液面上升,D管液面下降;
(5)写出实验IV中发生反应的离子方程式2Al+2H2O+2OH-=2AlO2-+3H2↑;若读数时C管液面低于D管液面,则测出的镁铝合金中镁的质量分数将偏高(填“偏高”、“偏低”或“无影响”).
| 实验 | A中试剂 | B中试剂 | C中液体 |
| I | 饱和食盐水 | 电石 | H2O |
| II | 浓氨水 | NaOH固体 | CCl4 |
| III | 生铁 | H2O | |
| IV | NaOH溶液 | 镁铝合金 | H2O |

(1)导管E的作用是:保持锥形瓶和分液漏斗间的压强恒定,使液体能顺利滴下、消除因液体的滴入引起的体积误差;
(2)实验I烧瓶B中发生反应的化学方程式是CaC2+2H2O→Ca(OH)2+C2H2↑,产生的气体经验纯后点燃,现象是火焰明亮并伴有浓烈的黑烟;
(3)实验Ⅱ剩余的NH3需吸收处理.以下各种尾气吸收装置中如图2,不能防止倒吸的是be;
(4)实验Ⅲ的实验目的是验证生铁在潮湿空气中会发生吸氧腐蚀.则A中试剂可选用ac(填序号);
a.NaOH溶液 b.C2H5OH c.NaCl溶液 d.稀硫酸
能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是C管的液面上升,D管液面下降;
(5)写出实验IV中发生反应的离子方程式2Al+2H2O+2OH-=2AlO2-+3H2↑;若读数时C管液面低于D管液面,则测出的镁铝合金中镁的质量分数将偏高(填“偏高”、“偏低”或“无影响”).
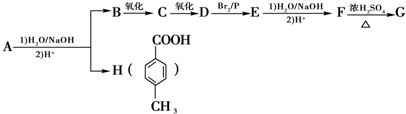
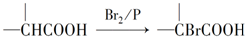
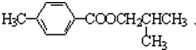 .
.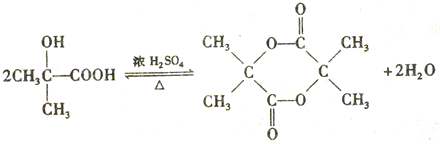 .
.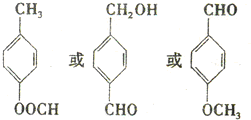 .
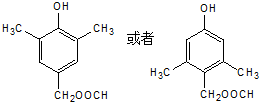
. )结构.
)结构.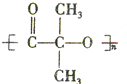 ,形成该聚合物的反应类型为:缩聚反应.
,形成该聚合物的反应类型为:缩聚反应.
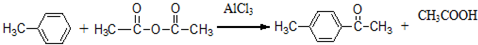
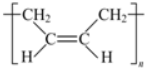 .
. .
. .
. .
. .
.