题目内容
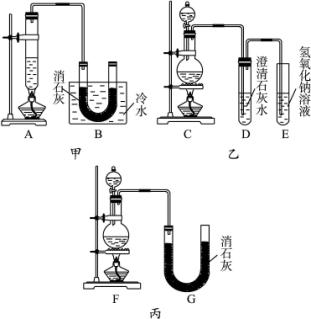
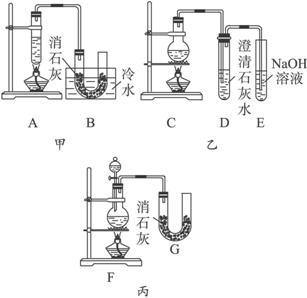
现用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉。已知反应2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O;ΔH<0,温度稍高即发生副反应6Cl2+6Ca(OH)2====5CaCl2+Ca(ClO3)2+6H2O。甲、乙、丙三人分别设计一个实验装置,如图所示。
(1)请指出三个装置各自的缺点或错误(如没有可不填):
甲__________________________________________________________。
乙__________________________________________________________。
丙__________________________________________________________。
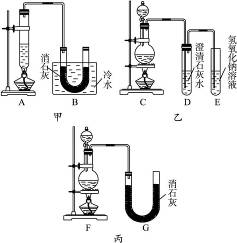
(2)图中甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号)______________。
(3)实验中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是小于0.15 mol,其可能的主要原因是____________________。(假定各步反应均无反应物损耗且无副反应发生)
(1)甲:①发生装置错误,②没有尾气吸收装置,③U形管右端不与大气相通,气体不能流动
乙:①没有冷却装置,②D应换成U形管,改装消石灰
丙:①没有冷却装置,②没有尾气吸收装置
(2)C(或F)、B、E
(3)MnO2只能氧化浓盐酸,随着反应进行,Cl-浓度减小,还原性减弱,反应不能继续进行
解析:
本题综合性较强,既要熟悉Cl2的实验室制法,又要抓住题给信息应用理论知识采取相应的实验措施。根据题给药品,制取Cl2应选用装置C或F。依据题给信息Cl2与Ca(OH)2反应是放热反应,且温度高时易发生副反应,所以制漂白粉时应采取降温措施。Cl2有毒,需进行尾气处理。

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案 Ca(ClO)2
Ca(ClO)2 5CaCl2
5CaCl2