题目内容
当光束通过下列分散系时,不能产生丁达尔效应的是( )
| A、雾 |
| B、Fe(OH)3胶体 |
| C、盐酸 |
| D、稀豆浆 |
考点:分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:分散系按照分散质粒度大小分为溶液、胶体、浊液.丁达尔效应是指:当一束光线透过胶体,从入射光的垂直方向可以观察到胶体里出现的一条光亮的“通路.丁达尔现象是胶体特有的性质,抓住这一特点即可解答.
解答:
解:A.雾分散质微粒直径在1-100nm之间,是胶体,属于气溶胶,有丁达尔效应,故A错误;
B.Fe(OH)3胶体分散质微粒直径在1-100nm之间,是胶体,有丁达尔效应,故B错误;
C.盐酸分散质微粒直径小于1nm是溶液,没有丁达尔效应,故C正确;
D.豆浆分散质微粒直径在1-100nm之间,属于胶体分散系,具有丁达尔现象,故D错误;
故选C.
B.Fe(OH)3胶体分散质微粒直径在1-100nm之间,是胶体,有丁达尔效应,故B错误;
C.盐酸分散质微粒直径小于1nm是溶液,没有丁达尔效应,故C正确;
D.豆浆分散质微粒直径在1-100nm之间,属于胶体分散系,具有丁达尔现象,故D错误;
故选C.
点评:本题考查了胶体的性质应用,注意丁达尔效应是胶体特有的性质是解答本题的关键,题目较简单.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是( )
| A、密闭容器中氨气的浓度不变 |
| B、密闭容器中总压强不变 |
| C、密闭容器中混合气体的密度不变 |
| D、2v(NH3)=v(CO2) |
下列说法中正确的是( )
| A、纯净的电解质在固态时全部属于离子晶体 |
| B、CCl4、CS2及BF3三种分子中所有原子都满足最外层8电子稳定结构 |
| C、用道尔顿的原子结构理论无法解释同位素现象 |
| D、化学键相同,则晶体类型也相同 |
在蒸发皿中加热蒸干并灼烧下列物质的溶液可以得到该物质的固体是( )
| A、Na2SO4 |
| B、NH4HCO3 |
| C、FeCl3 |
| D、Ca(HCO3)2 |
下列原子轨道表示式中,表示氧原子的基态电子轨道排布式正确的是( )
A、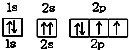 |
B、 |
C、 |
D、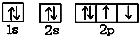 |
对电解质的叙述正确的是( )
| A、溶于水后得到的溶液能导电的物质 |
| B、熔融态能导电的物质 |
| C、电解所得到的物质 |
| D、在水溶液中或熔融状态下能导电的化合物 |
下列能用勒沙特列原理解释的是( )
| A、反应3NH4SCN+FeCl3?Fe(SCN)3+3NH4Cl平衡后,加入NH4Cl固体溶液颜色变深 |
| B、红棕色NO2加压后颜色先变深后变浅 |
| C、SO2氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混和气加压后颜色变深 |
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2.
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2.
| A、②④⑤ | B、①②④ |
| C、③⑤ | D、全部正确 |
把铜粉和铁粉的混合物放入一定量的稀硝酸中,微热,反应完毕发现铜有剩余,则溶液中含有的阳离子是( )
| A、Cu2+、Fe2+ |
| B、Cu2+、Fe2+、Fe3+ |
| C、Cu2+、Fe3+ |
| D、Fe3+ |