题目内容
9.铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物.(1)现有一含有FeCl2和FeCl3的混合物样品,测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为10%.
(2)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为2Fe3++2I-=2Fe2++I2.
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
分析 (1)依据元素守恒计算氯化亚铁和氯化铁物质的量之比,进一步计算氯化铁质量分数;
(2)氯化铁具有氧化性碘化氢具有还原性,二者发生氧化还原反应生成氯化亚铁和碘单质;
(3)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
解答 解:(1)FeCl2和FeCl3的混合物的样品中FeCl2物质的量为x,FeCl3的物质的量为y,则(x+y):(2x+3y)=1:2.1,得到x:y=9:1,氯化铁物质的量分数=$\frac{1}{1+9}$×100%=10%;故答案为:10%;
(2)氯化铁具有氧化性碘化氢具有还原性,二者发生氧化还原反应生成氯化亚铁和碘单质,反应离子方程式为:2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2;
(3)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,故答案为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
点评 本题考查学生阅读题目获取信息的能力、氧化还原反应,混合物质量分数计算,难度中等,要求学生要有扎实的基础知识和灵活运用知识解决问题的能力.注意基础知识的全面掌握.

练习册系列答案
相关题目
19.下列变化过程中,对外放热的是( )
①钢铁生锈
②酸碱中和
③浓硫酸稀释
④固体氢氧化钠溶于水
⑤H2在 Cl2中燃烧
⑥液态水变成 水蒸气
⑦NH4Cl 晶体与 Ba(OH)2•8H2O 混合搅拌
⑧工业制取水煤气.
①钢铁生锈
②酸碱中和
③浓硫酸稀释
④固体氢氧化钠溶于水
⑤H2在 Cl2中燃烧
⑥液态水变成 水蒸气
⑦NH4Cl 晶体与 Ba(OH)2•8H2O 混合搅拌
⑧工业制取水煤气.
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ②③④⑤ | D. | ①⑥⑦⑧ |
20.下列事实不能用元素周期律解释的只有( )
| A. | 碱性:KOH>NaOH | B. | 酸性:HClO4>H2SO4 | ||
| C. | 相对原子质量:Ar>K | D. | 元素的金属性:Mg>Al |
17.如图是某学生的过滤操作示意图,其操作不规范的是( )
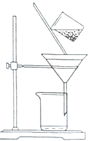

| A. | 漏斗末端颈尖未紧靠烧杯壁 | |
| B. | 玻璃棒用作引流 | |
| C. | 将滤纸湿润,使其紧贴漏斗壁 | |
| D. | 滤纸边缘高出漏斗 | |
| E. | 用玻璃棒在漏斗中轻轻搅动以加快过滤速度. |
14.可在火焰上直接加热的玻璃仪器是( )
| A. | 量筒 | B. | 试管 | C. | 圆底烧瓶 | D. | 烧杯 |
1.下列说法不正确的是( )
| A. | 乙酸具有酸的通性,能使紫色的石蕊溶液变红 | |
| B. | 在一定条件下,苯与液溴、浓硝酸作用生成溴苯、硝基苯的反应都属于取代反应 | |
| C. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| D. | 用溴水可以鉴别乙烯和乙烷 |
18.下列说法中正确的是( )
| A. | 物质的量就是物质的质量 | |
| B. | 摩尔是国际单位制中七个基本物理量之一 | |
| C. | 物质的量是量度物质所含微粒多少的一个物理量 | |
| D. | 1mol任何物质都含有6.02×1023个微粒 |
19.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Mg2+、Cl-、SO42- | |
| B. | 滴加石蕊试液显红色的溶液::K+、Al3+、Cl-、NO3- | |
| C. | 含有0.1mol•L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 无色透明的酸性溶液中:MnO4-、K+、SO42-、Na+ |



