题目内容
18.在48mL0.1mol/L硫酸溶液中加入4.7mL0.05mol/L氢氧化钠溶液,充分反应后,假若混合溶液的体积是酸、碱溶液体积的加和,则溶液中的c(H+)( )| A. | 0.9mol/L | B. | 0.18mol/L | C. | 0.42mol/L | D. | 0.84mol/L |
分析 先根据n=cV分别计算出硫酸中氢离子、氢氧化钠溶液中的氢氧根离子的物质的量,然后计算出混合液中氢离子物质的量,然后根据c=$\frac{n}{V}$计算出混合液中氢离子的物质的量浓度.
解答 解:48mL0.1mol/L硫酸溶液中含有氢离子的物质的量为:n(H+)=×0.048L×0.1mol/L×2=0.0096mol,
4.7mL0.05mol/L氢氧化钠溶液中氢氧根离子的物质的量为:n(OH-)=0.0047L×0.05mol/L=0.000235mol,
显然酸过量,混合液中氢离子浓度为:c(H+)=$\frac{0.0096mol-0.000235mol}{0.048L+0.0047L}$≈0.18mol/L,
故选B.
点评 本题考查了化学方程式的计算,题目难度不大,明确酸碱中和反应实质为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列化学用语表示正确的是( )
| A. | 铁原子的电子排布式:[Ar]3d64s2 | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 氢氧化钠的电子式: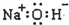 | D. | F的原子结构示意图: |
3.下列离子反应方程式正确的是( )
| A. | 在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++HCO3-+Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O | |
| B. | SO2气体通入Fe2(SO4)3溶液中:SO2+2H2O+2Fe3+=2Fe2++4H++SO42- | |
| C. | 用白醋除铁锈:Fe2O3•xH2O+6H+=(3+x)H2O+2Fe3+ | |
| D. | 硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-=NH3•H2O+H2O |
10.${\;}_{\;}^{16}$O和${\;}_{\;}^{18}$O是氧元素的两种核素,设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | ${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2互为同位素 | |
| B. | 等质量的${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2所含有的分子数相同 | |
| C. | 标准状况下,1.12L${\;}_{\;}^{16}$O2和1.12L${\;}_{\;}^{18}$O2均含有0.1NA个氧原子 | |
| D. | 通过化学变化可以实现${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2间的相互转化 |
7.胶体区别于其它分散系的特征是( )
| A. | 胶体粒子能够发生布朗运动 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子直径在1-100nm之间 | D. | 胶体粒子不能穿过半透膜 |
8.下列各组物质属同素异形体的是( )
| A. | 金刚石、石墨和C60 | B. | 16O和18O | ||
| C. | O2和SO3 | D. | H2O和H2O2 |