题目内容
17.下列实验事实的描述中,正确的是( )| A. | 除去苯中的苯酚可以加入过量浓溴水后过滤 | |
| B. | 向浓硫酸中缓慢加入乙醇和冰醋酸用以制备乙酸乙酯 | |
| C. | 向2mL 10% NaOH溶液中,加入2mL 2mol/L CuSO4溶液,振荡制Cu(OH)2悬浊液,用于检验醛的性质 | |
| D. | 加入Mg(OH)2固体可除去MgCl2溶液中混有的少量FeCl3 |
分析 A.三溴苯酚和溴都能够溶于苯,无法除去杂质;
B.应该先加入乙醇,然后再加入浓硫酸,最后加入乙酸,顺序不能颠倒;
C.制备Cu(OH)2悬浊液时氢氧化钠应该过量;
D.Mg(OH)2固体与铁离子水解生成的氢离子反应生成,促进三价铁水解.
解答 解:A.苯酚与浓溴水反应生成的三溴苯酚能够溶于苯,且溴也能够溶于苯,无法除去杂质,还引进了新的杂质,应该用氢氧化钠溶于,故A错误;
B.制备乙酸乙酯时,先加乙醇再加浓硫酸,最后加乙酸,故B错误;
C.制备Cu(OH)2悬浊液时氢氧化钠应该过量,使溶液显碱性,因为在碱性条件下Cu(OH)2悬浊液与醛基反应,故C错误;
D.Mg(OH)2固体与铁离子水解生成的氢离子反应生成,促进三价铁水解,使三价铁离子完全水解生成氢氧化铁沉淀,所以加入Mg(OH)2固体可除去MgCl2溶液中混有的少量FeCl3,故D正确;
故选D.
点评 本题考查实验方案的设计与评价,涉及除杂、乙酸乙酯的制备、盐的水解原理的应用等知识,题目难度中等,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
7.甲苯分子被溴原子取代一个氢原子后,可能形成的同分异构体的数目是( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
8.要将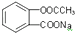 转化为
转化为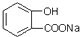 应选用的试剂和操作的是( )
应选用的试剂和操作的是( )
 转化为
转化为 应选用的试剂和操作的是( )
应选用的试剂和操作的是( )| A. | 加入足量的NaOH共热后,再通入足量的CO2 | |
| B. | 溶解,加热后通足量的CO2 | |
| C. | 与稀H2SO4共热后加足量的 NaOH | |
| D. | 与稀H2SO4共热后加足量的Na2CO3 |
5.下列元素非金属最强的是( )
| A. | S | B. | O | C. | Si | D. | P |
12.下列物质的分子中,不含共价键的是( )
| A. | MgCl2 | B. | Cl2 | C. | HCl | D. | NaOH |
2.醋酸铅因有甜味而被称为“铅糖”,它有毒但能入药,又知(CH3COO)2Pb可溶于水,硝酸铅与醋酸钠溶液反应的离子方程式为Pb2++2CH3COO-=(CH3COO)2Pb. 下列有关说法中不正确的是( )
| A. | 0.1 mol•L-1的“铅糖”溶液中c(Pb2+)<0.1 mol•L-1 | |
| B. | “铅糖”是强电解质 | |
| C. | “铅糖”是共价化合物 | |
| D. | “铅糖”的溶液可能不导电 |
9.下列粒子半径最大的是( )
| A. | Na+ | B. | Al3+ | C. | S2- | D. | Cl- |
6.下列离子方程式正确的是( )
| A. | 将氯气通入氢氧化钡溶液中:Cl2+2 OH-=H2O+Cl-+ClO- | |
| B. | 贝壳溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| C. | 铁与FeCl3溶液反应:Fe+Fe3+=2Fe2+ | |
| D. | 硫酸溶液与氢氧化钡溶液混合:Ba2++OH -+H++SO42-=BaSO4↓+H2O |
2.下列除杂方法可行的是AD
| 选项 | 物质(括号内为杂质) | 除杂试剂 |
| A | CO(CO2) | 通入过量澄清石灰水 |
| B | CaCl2溶液(HCl) | 加适量Ba(OH)2溶液 |
| C | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| D | NaOH溶液(Na2CO3) | 加适量Ca(OH)2或Ba(OH)2溶液、过滤 |