题目内容
(l)某地酸雨中可能含有下列离子:Na+、Mg2+、NH4+、Cl-、S0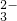 S0
S0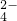 、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0
、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0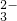 的实验操作是______(填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是______;
的实验操作是______(填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是______;
A.取试样,滴加适量的淀粉KI溶液,呈蓝色:
B.取试样,滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;
C.取试样,滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝:
D.取试样,滴加酸性KMnO4溶液,不褪色.
(2)某溶液含两种相同物质的量的溶质,且溶液中只存在OH-、H+、NH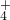 、Cl-四种离子,其中c(NH
、Cl-四种离子,其中c(NH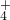 )>c(Cl-)则这两种溶质的化学式分别是______.
)>c(Cl-)则这两种溶质的化学式分别是______.
(3)已知25℃时Ksp(RX)=1.8X 10-10,Ksp(RY)=1.8X 10-16,Ksp(R2Z)=1.8X 10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是______.
解:(1)A.滴加适量的淀粉KI溶液,呈蓝色,说明存在氧化性离子N03-,所以没有SO32-;
D.取试样,滴加酸性KMnO4溶液,不褪色,说明没有还原性离子SO32-,故答案为A或D;
因为N02-能够被酸性KMnO4溶液氧化,而使KMnO4溶液褪色,而实验D中KMnO4溶液不褪色,所以不含N02-,故答案为:不含有,若有N02-,能使酸性KMnO4溶液褪色;
(2)根据电荷守恒c(Cl-)+c(OH-)=c(H+)+c(NH4+),c(NH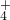 )>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,所以溶质为NH4Cl和NH3?H2O,故答案为NH4Cl和NH3?H2O;
)>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,所以溶质为NH4Cl和NH3?H2O,故答案为NH4Cl和NH3?H2O;
(3)RX中c(R+)=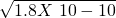 ,RY中c(R+)=
,RY中c(R+)=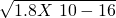 ,R2Z中c(R+)=
,R2Z中c(R+)=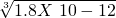 ,故答案为R2Z>RX>RY.
,故答案为R2Z>RX>RY.
分析:(1)A.滴加适量的淀粉KI溶液,呈蓝色,说明存在氧化性离子N03-,所以没有SO32-;
D.取试样,滴加酸性KMnO4溶液,不褪色,说明没有还原性离子SO32-;
因为N02-能够被酸性KMnO4溶液氧化,而使KMnO4溶液褪色,而实验D中KMnO4溶液不褪色,所以不含N02-;
(2)根据电荷守恒c(Cl-)+c(OH-)=c(H+)+c(NH4+),c(NH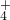 )>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,故溶质为NH4Cl和NH3?H2O;
)>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,故溶质为NH4Cl和NH3?H2O;
(3)RX中c(R+)=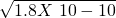 ,RY中c(R+)=
,RY中c(R+)=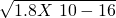 ,R2Z中c(R+)=
,R2Z中c(R+)=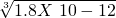 .
.
点评:本题考查了几种常见离子的检验方法,以及电荷守恒的应用和Ksp的简单计算.
D.取试样,滴加酸性KMnO4溶液,不褪色,说明没有还原性离子SO32-,故答案为A或D;
因为N02-能够被酸性KMnO4溶液氧化,而使KMnO4溶液褪色,而实验D中KMnO4溶液不褪色,所以不含N02-,故答案为:不含有,若有N02-,能使酸性KMnO4溶液褪色;
(2)根据电荷守恒c(Cl-)+c(OH-)=c(H+)+c(NH4+),c(NH
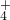 )>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,所以溶质为NH4Cl和NH3?H2O,故答案为NH4Cl和NH3?H2O;
)>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,所以溶质为NH4Cl和NH3?H2O,故答案为NH4Cl和NH3?H2O;(3)RX中c(R+)=
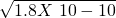 ,RY中c(R+)=
,RY中c(R+)=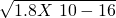 ,R2Z中c(R+)=
,R2Z中c(R+)=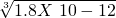 ,故答案为R2Z>RX>RY.
,故答案为R2Z>RX>RY.分析:(1)A.滴加适量的淀粉KI溶液,呈蓝色,说明存在氧化性离子N03-,所以没有SO32-;
D.取试样,滴加酸性KMnO4溶液,不褪色,说明没有还原性离子SO32-;
因为N02-能够被酸性KMnO4溶液氧化,而使KMnO4溶液褪色,而实验D中KMnO4溶液不褪色,所以不含N02-;
(2)根据电荷守恒c(Cl-)+c(OH-)=c(H+)+c(NH4+),c(NH
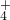 )>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,故溶质为NH4Cl和NH3?H2O;
)>c(Cl-) 所以c(H+)<c(OH-)即溶液显碱性,故溶质为NH4Cl和NH3?H2O;(3)RX中c(R+)=
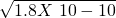 ,RY中c(R+)=
,RY中c(R+)=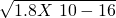 ,R2Z中c(R+)=
,R2Z中c(R+)=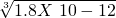 .
.点评:本题考查了几种常见离子的检验方法,以及电荷守恒的应用和Ksp的简单计算.

练习册系列答案
相关题目

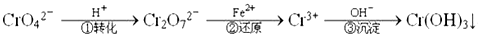
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O  Cr3+(aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_____。
Cr3+(aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_____。  S0
S0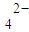 、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0
、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0 的实验操作是 (填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是 ;
的实验操作是 (填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是 ; 、Cl-四种离子,其中c(NH
、Cl-四种离子,其中c(NH )>c(Cl-)则这两种溶质的化学式分别是 .
)>c(Cl-)则这两种溶质的化学式分别是 .