题目内容
下列分子的中心原子发生sp2杂化的是( )
分析:根据分子的组成判断形成的δ键数目以及孤电子对数目,以此判断杂化类型.
解答:解:A.CH4中C形成4个δ键,无孤电子对,为sp3杂化,故A错误;
B.NH3中N形成3个δ键,孤电子对数=
=1,为sp3杂化,故B错误;
C.H2O中O形成2个δ键,孤电子对数=
=2,为sp3杂化,故C错误;
D.BF3中B形成3个δ键,无孤电子对,为sp2杂化,故D正确.
故选D.
B.NH3中N形成3个δ键,孤电子对数=
| 5-3×1 |
| 2 |
C.H2O中O形成2个δ键,孤电子对数=
| 6-2×1 |
| 2 |
D.BF3中B形成3个δ键,无孤电子对,为sp2杂化,故D正确.
故选D.
点评:本题考查杂化类型的判断,题目难度不大,注意根据δ键数目以及孤电子对数目进行判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
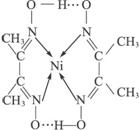 分子内的作用力有____________(填编号)。
分子内的作用力有____________(填编号)。
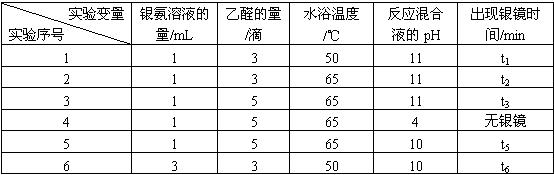 请回答下列问题:
请回答下列问题: