题目内容
17.利用反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H,可减少CO2排放,并合成清洁能源.500℃时,在容积为2L的密闭容器中充入2molCO2和6molH2,测得t=5min时,反应达到平衡,此时n(CO2)=0.5mol.
①从反应开始到平衡,H2的平均反应速率v(H2)=0.45mol/(L•min);该可逆反应的平衡常数为5.33(结果保留两位有效数字);平衡时H2的转化率为75%.
②若将上述平衡体系的温度升高至800℃达到新平衡,平衡常数K为5.0,该反应的△H<(填“>”、“<”或“=”)0.
③已知上数条件下H2的平衡转化率为a,如果将恒容条件改成恒压条件,H2的平衡转化率为b.则a<(填“>”、“<”或“=”)b.
分析 结合化学反应三行计算列式,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 1 3 0 0
变化硫(mol/L) 0.75 2.25 0.75 0.75
平衡量(mol/L) 0.25 0.75 0.75 0.75
①反应速率v=$\frac{△c}{△t}$,平衡常数K=$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{c(C{O}_{2}){c}^{3}({H}_{2})}$,转化率=$\frac{消耗量}{起始量}$×100%;
②和①计算得到平衡常数比较,随温度升高平衡常数减小,则正反应为放热反应,若随温度升高增大,则正反应为吸热反应;
③如果将恒容条件改成恒压条件,反应前后气体体积减小,所以恒压条件下为保持恒压,压强大于恒容,平衡正向进行氢气转化率增大;
解答 解:结合化学反应三行计算列式,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 1 3 0 0
变化硫(mol/L) 0.75 2.25 0.75 0.75
平衡量(mol/L) 0.25 0.75 0.75 0.75
①从反应开始到平衡,H2的反应速率v=$\frac{△c}{△t}$=$\frac{2.25mol/L}{5min}$=0.45mol/(L•min),
平衡常数K=$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{c(C{O}_{2}){c}^{3}({H}_{2})}$=$\frac{0.75×0.75}{0.25×0.7{5}^{3}}$=5.33,
平衡时H2的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{2.25mol/L}{3mol/L}$×100%=75%,
故答案为:=0.45mol/(L•min);5.33;75%;
②若将上述平衡体系的温度升高至800℃达到新平衡,平衡常数K为5.0,和①计算得到平衡常数,随温度升高K减小,则正反应为放热反应,△H<0,
故答案为:<;
③如果将恒容条件改成恒压条件,反应前后气体体积减小,所以恒压条件下为保持恒压,压强大于恒容,平衡正向进行氢气转化率增大,
故答案为:<.
点评 本题考查了化学反应速率、平衡常数、转化率计算应用,主要是平衡常数和反应速率影响因素的理解应用,题目难度中等.

| A. | 同主族元素从上到下,其氢化物的稳定性逐渐增强 | |
| B. | 同周期元素(0族除外) 从左到右,原子半径逐渐减小 | |
| C. | 将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 | |
| D. | Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 |
| A. | 0.1mol/L Na2CO3溶液:c(OH-)+c(H+)═c(HCO3-)+2c(H2CO3) | |
| B. | 0.1mol/L NH4Cl溶液:c(NH4+)+c(Cl-)═0.2mol/L | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=4的混合溶液:c(Na+)═c(NO3-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
| A. | 金属钠 | B. | 浓硫酸 | C. | 银氨溶液 | D. | 氢氧化钠 |
(1)常温下,用CO、O2和水在三苯基膦钯的催化下即可制得H2O2.相对于电解氢氧化钠溶液制H2O2,该方法具有的优点是安全、能耗低.
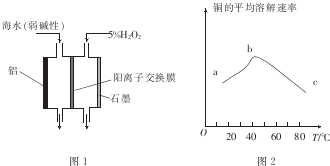
(2)图1是铝/过氧化氢电池结构示意图.铝电极为负极(填“正极”或“负极”),石墨电极的电极反应式为H2O2+2e-=2OH-
(3)印刷电路板中的金属铜可用10%的H2O2溶液和3.0mol.L-l的H2S04溶液处理,其他条件相同时,测得铜的平均溶解速率与温度的关系如图2所示.其中bc段曲线变化的主要原因是随着温度的升高,双氧水的分解速率加快
(4)为研究硫酸铁的量对过氧化氢分解速率的影响,某同学设计了如下一系列的实验.将表中所给的溶液分别加入A、B、C、D 4个反应瓶中,收集产生的气体,记录数据.
| 实验 体积/mL 液体 | A | B | C | D |
| 0.4mol.L-1Fe2(SO4)3溶液 | 0 | 1.8 | 2.0 | V1 |
| 30%H2O2溶液 | 20.0 | 20.0 | 20.0 | 20.0 |
| HO2 | V2 | V3 | 15.0 | 13.8 |
②上表中V3=15.2.
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:Cl>S | ||
| C. | 热稳定性Na2CO3>NaHCO3 | D. | 碱性:NaOH>Mg(OH)2 |
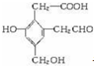 ,试回答:
,试回答: