题目内容
下列叙述中正确的是( )
| A、原电池跟电解池连接后,电子从电池负极流向电解池阳极 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分 |
| D、工业上铜的电解精炼时电解池中每转移1mol电子时阴极析出的铜小于0.5NA |
考点:原电池和电解池的工作原理,铜的电解精炼,氯、溴、碘及其化合物的综合应用
专题:电化学专题,卤族元素
分析:A、与原电池的负极相连的为电解池的阴极;
B、减少生成物的浓度,反应速率减小;
C、电解饱和NaCl溶液生成氯气、氢气和氢氧化钠;
D、电解精炼时阴极铜离子得电子生成Cu.
B、减少生成物的浓度,反应速率减小;
C、电解饱和NaCl溶液生成氯气、氢气和氢氧化钠;
D、电解精炼时阴极铜离子得电子生成Cu.
解答:
解:A、与原电池的负极相连的为电解池的阴极,则原电池跟电解池连接后,电子从电池负极流向电解池阴极,故A错误;
B、减少生成物的浓度,反应速率减小,则合成氨生产过程中将NH3液化分离,减小正反应速率,平衡正移,提高N2、H2的转化率,故B错误;
C、电解饱和NaCl溶液生成氯气、氢气和氢氧化钠,氯气与氢氧化钠反应生成次氯酸钠,次氯酸钠是“84”消毒液中的有效成分,故C正确;
D、电解精炼时阴极铜离子得电子生成Cu,阴极电极反应为Cu2++2e-=Cu,则每转移1mol电子时阴极析出的铜为0.5NA,故D错误.
故选C.
B、减少生成物的浓度,反应速率减小,则合成氨生产过程中将NH3液化分离,减小正反应速率,平衡正移,提高N2、H2的转化率,故B错误;
C、电解饱和NaCl溶液生成氯气、氢气和氢氧化钠,氯气与氢氧化钠反应生成次氯酸钠,次氯酸钠是“84”消毒液中的有效成分,故C正确;
D、电解精炼时阴极铜离子得电子生成Cu,阴极电极反应为Cu2++2e-=Cu,则每转移1mol电子时阴极析出的铜为0.5NA,故D错误.
故选C.
点评:本题考查了原电池原理和电解池原理的应用、反应速率和化学平衡,题目涉及的知识点较多,侧重于考查学生对基础知识的应用能力,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
n种炔烃与足量的氢气催化加成得到m种烷烃,且烷烃满足的条件:①主链含5个碳原子②两个支链:一个甲基、一个乙基.n、m的最大值分别为( )
| A、2、2 | B、2、4 |
| C、4、2 | D、4、5 |
对于在一定条件下的放热反应来说,升高温度( )
| A、正反应速率加快 |
| B、逆反应速率加快 |
| C、正、逆反应速率都加快 |
| D、正反应速率减慢,逆反应速率加快 |
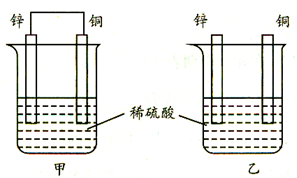 将纯铜片和纯锌片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
将纯铜片和纯锌片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中铜片是正极,电极反应:2H++2e→H2↑;乙中锌片是负极,电极反应:Zn-2e→Zn2+ |
| C、两烧杯中的pH值均增大 |
| D、产生的气泡速率甲比乙慢 |
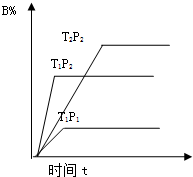 已知某可逆反应:mA(g)+nB(g)═pC(g)在密闭容器中进行,如图表示反应在不同时间t、温度T和压强P与反应物B在混合气体的体积分
已知某可逆反应:mA(g)+nB(g)═pC(g)在密闭容器中进行,如图表示反应在不同时间t、温度T和压强P与反应物B在混合气体的体积分数(B%)的关系曲线.由曲线分析下列判断正确的是( )
| A、T1<T2 P1>P2m+n>p 正反应为吸热反应 |
| B、T1>T2 P2>P1 m+n<p 正反应为吸热反应 |
| C、T2>T1 P2>P1m+n<p 正反应为吸热反应 |
| D、T1>T2 P2>P1 m+n<p 正反应为放热反应 |
下列物质性质与应用对应关系正确的是( )
| A、漂白粉在空气中不稳定,可用于漂白纸张 |
| B、医用酒精能使蛋白质变性,可用于消毒杀菌 |
| C、二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| D、铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀 |
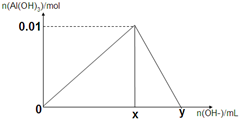 将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题:
将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题: