题目内容
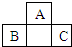 如图是元素周期表短周期的一部分,已知B原子与C原子核外电子总数和为A原子核外电子总数的4倍,则以下推断正确的是( )
如图是元素周期表短周期的一部分,已知B原子与C原子核外电子总数和为A原子核外电子总数的4倍,则以下推断正确的是( )| A、三者皆为非金属元素 |
| B、B与A、B与C均可以形成离子化合物 |
| C、三者核电荷数之和为40 |
| D、B与C只能形成一种共价化合物 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素在周期表中位置,可A处于第二周期,B、C处于第三周期,已知B原子与C原子核外电子总数之和为A的4倍,设A的原子序数x,则B的原子序数为x+7,C的原子序数为x+9,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为Cl,以此来解答.
解答:
解:由短周期元素在周期表中位置,可A处于第二周期,B、C处于第三周期,已知B原子与C原子核外电子总数之和为A的4倍,设A的原子序数x,则B的原子序数为x+7,C的原子序数为x+9,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为Cl,
A.A为O元素,B为P元素,C为Cl元素,三种元素都是非金属,故A正确;
B.P与O、P与Cl均可以形成共价化合物,故B错误;
C.三者核电核数之和为8+15+17=40,故C正确;
D.P与Cl可以形成PCl3、PCl5,故D错误,
故选AC.
A.A为O元素,B为P元素,C为Cl元素,三种元素都是非金属,故A正确;
B.P与O、P与Cl均可以形成共价化合物,故B错误;
C.三者核电核数之和为8+15+17=40,故C正确;
D.P与Cl可以形成PCl3、PCl5,故D错误,
故选AC.
点评:本题考查结构性质位置关系的应用,难度不大,推断元素是解题关键,注意理解同主族元素原子序数关系.

练习册系列答案
相关题目
下列关于热化学反应的描述中正确的是( )
| A、CO燃烧是吸热反应 |
| B、需要加热才能发生的反应一定是吸热反应 |
| C、CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)的反应热为△H=+2×283.0kJ/mol |
| D、1mol CH4燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为1NA |
| B、常温常压下,106gNa2CO3含有的Na+离子数为2NA |
| C、通常状况下,1NA个CO2分子占有的体积为22.4L |
| D、物质的量浓度为0.5mol?/L的MgCl2溶液中,含有Cl-个数为1NA |
下列装置或操作错误,不能达到实验目的是( )
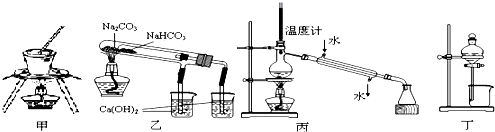

| A、用甲图装置可用于加热、灼烧固体 |
| B、用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C、用丙图装置分离乙醇与水 |
| D、用丁图装置可由四氯化碳萃取碘水中的碘 |
下列说法中不正确的是( )
| A、二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
B、结构简式为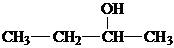 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 |
| C、分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 |
D、某有机物球棍结构模型为: ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 |
气态反应A(g)+3B(g)═2C(g)+2D(g),在四种不同条件下的反应速率如下,其中反应速率最快的是( )
| A、vA=0.15 mol/(L?min) |
| B、vB=0.6 mol/(L?min) |
| C、vC=0.4 mol/(L?min) |
| D、vD=0.6 mol/(L?min) |
在0.1mol/L的氨水中存在 NH3?H2O?NH4++OH-的电离平衡,下列措施都能使 该平衡向右移动的一组是( )
①加入少量HCl;②加入固体NaOH;③加水;④通入氨气;⑤加热升高温度;⑥加入NH4NO3.
①加入少量HCl;②加入固体NaOH;③加水;④通入氨气;⑤加热升高温度;⑥加入NH4NO3.
| A、①③④⑤ | B、①③④⑤⑥ |
| C、②③④⑤ | D、①③④⑥ |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )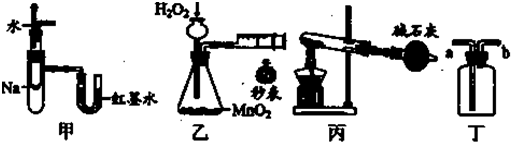

| A、装置甲可用于验证反应的热效应 |
| B、装置乙可定量测定化学反应的速率 |
| C、装置丙可用于实验室以NH4Cl为原料制备少量NH3 |
| D、装置丁a口进气可收集NH3、C12等气体 |
下列物质:①Hg(NO3)2 ②HCHO(甲醛) ③MgSO4 ④NH4Cl ⑤KOH中,能使蛋白质变性的是( )
| A、②③④ | B、①③⑤ |
| C、①②③ | D、①②⑤ |