题目内容
3. 煤的气化在煤化工业中占有重要地位,至今仍然是化学工业的重要组成部分.
煤的气化在煤化工业中占有重要地位,至今仍然是化学工业的重要组成部分.(1)已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.请写出CH3OH(l)完全燃烧生成二氧化碳和液态水的热化学方程式:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1.
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度/℃ | 250 | 300 | 350 |
| K/L2•mol-2 | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,4min达到平衡时测得c(CO)=0.2mol/L,此时的温度为250℃,则反应速率v(H2)=0.4mol•L-1•min-1.
(3)T℃时,在t0时刻,合成甲醇反应CO(g)+2H2(g)?CH3OH(g)达到平衡,若在t1时刻将容器的体积缩小为原来的$\frac{1}{2}$,在t2时刻又达到新的平衡,请在图中用曲线表示t1~t2时间段氢气、甲醇物质的量浓度随时间变化的趋势示意图(其他条件不变,曲线上必须标明氢气、甲醇).
(4)如果用CH3OH和空气作燃料电池,用KOH作电解质溶液,请写出该燃料电池的负极的电极反应式CH3OH-6e-+8OH-=CO32-+6H2O.
分析 (1)已知CH3OH(l)的燃烧热为-726.5kJ/mol,据此书写CH3OH完全燃烧生成二氧化碳和液态水的热化学方程式;
(2)①平衡常数为生成物浓度的幂次方之积比上反应物浓度的幂次方之积;升高温度,可逆反应向吸热反应方向移动,根据平衡常数与温度变化关系确定焓变;
②根据平衡浓度计算出平衡常数来确定温度;根据v=$\frac{△c}{△t}$计算反应速率;
(3)若在t1时刻将容器的体积缩小为原来的$\frac{1}{2}$,相当于增大压强,各组分的浓度立即增加原来的一倍,然后是平衡开始正向移动,据此分析;
(4)燃料电池的负极CH3OH失电子发生氧化反应.
解答 解:(1)已知CH3OH(l)的燃烧热为-726.5kJ/mol,则CH3OH完全燃烧生成二氧化碳和液态水的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1,故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1;
(2)①平衡常数为生成物浓度的幂次方之积比上反应物浓度的幂次方之积,则CO(g)+2H2(g)?CH3OH(g)反应的平衡常数的表达式K=$\frac{c(CH{\;}_{3}OH)}{c(CO)•c{\;}^{2}(H{\;}_{2})}$,升高温度,平衡向吸热方向移动,根据表格知,温度越高,化学平衡常数越小,说明平衡向逆反应方向移动,所以正反应是放热反应,即△H<0,
故答案为:K=$\frac{c(CH{\;}_{3}OH)}{c(CO)•c{\;}^{2}(H{\;}_{2})}$;<;
②CO(g)+2H2(g)?CH3OH(g)
开始 1mol/L 3mol/L 0
转化 0.8mol/L 1.6mol/L 0.8mol/L
平衡 0.2mol/L 1.4mol/L 0.8mol/L
平衡常数K=$\frac{0.8}{0.2×1.4{\;}^{2}}$=2.04,所以是250℃;反应速率v(H2)=$\frac{1.6mol/L}{4min}$=0.4mol•L-1•min-1,故答案为:250℃;0.4mol•L-1•min-1;
(3)若在t1时刻将容器的体积缩小为原来的$\frac{1}{2}$,相当于增大压强,各组分的浓度立即增加原来的一倍,然后是平衡开始正向移动,至t2时刻又达到新的平衡,图示如下: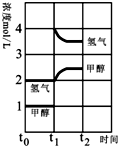 ;故答案为:
;故答案为: ;
;
(4)用CH3OH和空气作燃料电池,用KOH作电解质溶液,负极CH3OH失电子发生氧化反应,则负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O.
点评 本题考查了影响化学平衡移动的因素、速率的计算、热化学方程式以及电极反应式的书写等知识点,综合性强,难度大,有利于提高学生的分析能力及灵活应用能力.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案| A. | H2CO3═2H++CO32- | B. | NaHSO4═Na++HSO4- | ||
| C. | NaHCO3?Na++HCO3- | D. | Ba(OH)2═Ba2++2OH- |
| A. | 在含有大量Fe3+的溶液中:Na+,SCN-,SO42-,NO3- | |
| B. | 在pH=1的溶液中:Fe3+,Mg2+,Cl-,SO42- | |
| C. | 在加入了FeSO4•7H2O晶体溶液中:Na+,H+,Cl-,NO3- | |
| D. | 能使紫色石蕊试液变红的溶液中:K+,HCO3-,NO3-,S2- |
| 实验设计 | 预期目的 | |
| A | 在相同温度下,分别取等质量的大理石块、大理石粉末分别与等体积等浓度的稀硫酸反应 | 探究反应物接触面积对化学反应速率的影响 |
| B | 把盛有颜色相同的NO2和N2O4的混合气体的两支试管(密封)分别浸入冷水和热水中 | 探究温度对化学平衡的影响 |
| C | 将铁棒和石墨用导线连接后插入含有Fe2+、Cu2+的盐溶液中 | 探究Fe2+和Cu2+的氧化性相对强弱 |
| D | 相同温度下,向两支盛有等体积等浓度H2O2溶液的试管中分别滴入适量的CuSO4溶液和FeCl3溶液 | 探究不同催化剂对同一反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| B. | 酒精、硫酸钡和水分别属于电解质、强电解质和弱电解质 | |
| C. | 胶体区别于其它分散系的本质特性是具有丁达尔现象 | |
| D. | 利用半透膜可除去淀粉溶液中的少量NaCl |
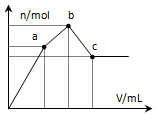 向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A. | a点的溶液呈中性 | |
| B. | 从开始到b点发生反应的总的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ | |
| C. | c点加入Ba(OH)2溶液的体积为200 mL | |
| D. | c点溶液呈碱性 |
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
| a | ||||
| b | ||||
| c | d | |||
| e |
| A. | b元素除0价外,只有一种化合价 | |
| B. | c元素只能形成一种氢化物且很不稳定 | |
| C. | d元素是五种元素中原子半径最小的一种 | |
| D. | e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐 |
