��Ŀ����
2��A��B��C��D��Ϊ������Ԫ�أ�ԭ����������������֪����A��Dͬ���壬A�γɵ��⻯�����M��D�γɵ��⻯�����N������18�����ӣ���һ�������£�A��D�ֱ��B�γɵĻ�����X��Y������ͬ��Ħ������������ɫ��Ӧ���ʻ�ɫ����A��C�γɵĻ�����Z���γ�ԭ�Ӿ��壮��ش��������⣺��1��X�ĵ���ʽΪ
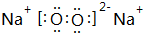 ��Z�Ļ�ѧʽΪSiO2��
��Z�Ļ�ѧʽΪSiO2����2��A��B��C��D����Ԫ�ص�ԭ�Ӱ뾶����С�������е�˳��Ϊ��Na��Si��S��O����Ԫ�ط��ű�ʾ����
��3��������Y��ˮ��ҺpH��7�������ӷ���ʽ˵��ԭ��S2-+H2O?HS-+OH-��
��4����M����Һ��ͨ��N���ɷ�����Ӧ����D�ĵ��ʺ�A����һ���⻯���д����ѧ����ʽH2O2+H2S=S��+2H2O��
���� A��B��C��D��Ϊ������Ԫ�أ�ԭ��������������A��Dͬ���壬A�γɵ��⻯�����M��D�γɵ��⻯�����N������18�����ӣ���AΪOԪ�ء�NΪSԪ�أ�MΪH2O2��DΪH2S��
��һ�������£�A��D�ֱ��B�γɵĻ�����X��Y������ͬ��Ħ������������ɫ��Ӧ���ʻ�ɫ����BΪNa��XΪNa2O2��YΪNa2S��
��A��C�γɵĻ�����Z�ǹ��ά����Ҫԭ�ϣ���CΪSi��ZΪSiO2��
��� �⣺A��B��C��D��Ϊ������Ԫ�أ�ԭ��������������
��A��Dͬ���壬A�γɵ��⻯�����M��D�γɵ��⻯�����N������18�����ӣ���AΪOԪ�ء�DΪSԪ�أ�MΪH2O2��NΪH2S��
��һ�������£�A��D�ֱ��B�γɵĻ�����X��Y������ͬ��Ħ������������ɫ��Ӧ���ʻ�ɫ����BΪNa��XΪNa2O2��YΪNa2S��
��A��C�γɵĻ�����Z�ǹ��ά����Ҫԭ�ϣ���CΪSi��ZΪSiO2��
��1��XΪNa2O2������ʽΪ ��Z�Ļ�ѧʽΪSiO2��
��Z�Ļ�ѧʽΪSiO2��
�ʴ�Ϊ�� ��SiO2��
��SiO2��
��2��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��Na��Si��S��O��
�ʴ�Ϊ��Na��Si��S��O��
��3��YΪNa2S����Һ��������ˮ����Һ�ʼ��ԣ����ӷ���ʽ�ǣ�S2-+H2O?HS-+OH-��
�ʴ�Ϊ��S2-+H2O?HS-+OH-��
��4����H2O2����Һ��ͨ��H2S����Ӧ��������ˮ����Ӧ����ʽΪ��H2O2+H2S=S��+2H2O��
�ʴ�Ϊ��H2O2+H2S=S��+2H2O��
���� ���⿼��Ԫ�ػ������ƶϣ�ע�������ɫ��Ӧ��18���ӽ����ƶϣ�����������ѧ����10���ӡ�18��������

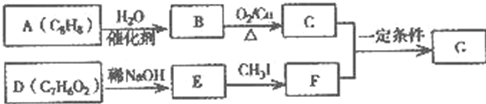
| A�� | ����ʽΪC7H16������������3������ͬ���칹����2�� | |
| B�� | ����ʽΪC7H12O4������ֻ������-COOCH3���ŵ�ͬ���칹�壨�����������칹������4�� | |
| C�� | 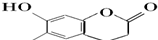 ���Ӵ��Ľṹ��ʽ��ͼ�÷�������5�ֹ����� ���Ӵ��Ľṹ��ʽ��ͼ�÷�������5�ֹ����� | |
| D�� | 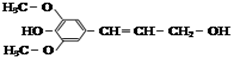 ��������ͼ��ʹ���Ը��������Һ��ɫ����1mol������4mol����������Ӧ |
| A�� | c��F-����c��OH-����c��HCN����c��HF�� | B�� | c��F-��+c��HF����c��CN-��+c��HCN�� | ||
| C�� | c��OH-����c��F-����c��CN-����c��H+�� | D�� | c��OH-����c��HF����c��HCN����c��H+�� |
| A�� | ���м���Ũ��ˮ�����ۣ����ȣ��ټ���AgNO3��Һ������������˵������Ũ��ˮ������ȡ����Ӧ | |
| B�� | ʵ�����Ʊ�����Ȳ����ͨ������һ���Ĵ̼�����ζ������ͨ��NaOH��Һ��Ũ����ϴ������ô�������Ȳ | |
| C�� | ��2%��AgNO3��Һ����εμ�2%�İ�ˮ��ֱ�������İ�ɫ����ǡ����ʧ�������Ƶõ�������Һ | |
| D�� | ��NaOH��Һ�м��������飬���ȣ��ټ���AgNO3��Һ������������˵�������鷢����ˮ�ⷴӦ |
 2015��8��12�Žӽ���ҹʱ�֣�����������һ����װ����ͷ������ը��������ը���Ǽ�װ���ڵ���ȼ�ױ���Ʒ����ը������죬��������Ģ���ƣ��������յ���Ϣ������װ������Σ�ջ�ѧƷ�����мء��ơ������ơ�����ء��ռ��軯�ơ�������ϩ���ȵ���ȣ��˵�����Σ�ջ�ѧƷ�����л����������������ᡢ����李��軯�ơ�4��6-��������-���ٶ������ӵȣ�
2015��8��12�Žӽ���ҹʱ�֣�����������һ����װ����ͷ������ը��������ը���Ǽ�װ���ڵ���ȼ�ױ���Ʒ����ը������죬��������Ģ���ƣ��������յ���Ϣ������װ������Σ�ջ�ѧƷ�����мء��ơ������ơ�����ء��ռ��軯�ơ�������ϩ���ȵ���ȣ��˵�����Σ�ջ�ѧƷ�����л����������������ᡢ����李��軯�ơ�4��6-��������-���ٶ������ӵȣ�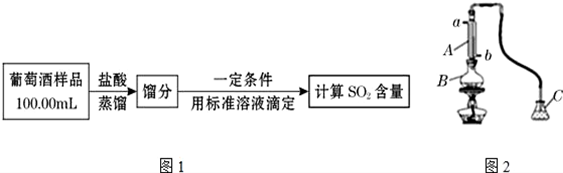

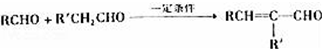
 ��
�� ��
��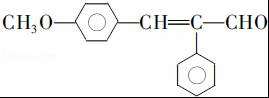 ��
��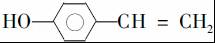 ��д�ṹ��ʽ����
��д�ṹ��ʽ����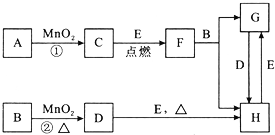
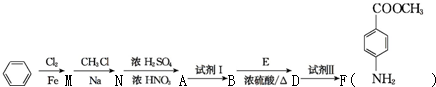
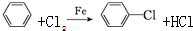
 �����������ԣ���������
�����������ԣ���������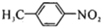 ��
��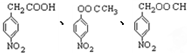 ����2�֣�
����2�֣�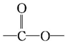 �ṹ��
�ṹ��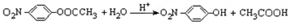 ��
��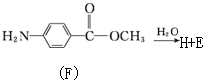 ������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ
������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ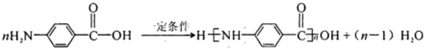 ��
��