题目内容
8.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| B. | 标准状况下,2.24L NO与11.2L O2混合后气体的分子数小于NA | |
| C. | 120g熔融的NaHSO4中含阳离子总数为2NA | |
| D. | 用5mL 3mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015NA |
分析 A、依据碳酸钠水解显碱性,结合溶液中离子积常数计算分析,溶液体积不知不能计算微粒数;
B.由2NO+O2═2NO2,2NO2?N2O4,利用气体的物质的量来分析分子总数;
C.熔融的NaHSO4中含有的阳离子只有钠离子;
D.一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答 解:A、25℃,pH=11的Na2CO3溶液中存在离子积常数,[H+]余=10-11mol/L;[H+]余•[OH-]水=10-14 ;由水电离出的[H+]=[OH-]=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3mol/L;溶液体积不知,由水电离出的氢离子的数目无法计算,故A错误;
B.标准状况下,22.4LNO和11.2L氧气的物质的量分别为1mol、0.5mol,由2NO+O2═2NO2、2NO2?N2O4,则气体的分子总数小于NA个,故B正确;
C.120g熔融的NaHSO4的物质的量为1mol,1mol熔融硫酸氢钠电离出1mol钠离子和1mol硫酸氢根离子,所以含有的阳离子数为NA,故C错误;
D.一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故所含胶粒的个数小于0.015NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,题目难度中等,应注意公式的运用和物质的结构特点,掌握基础是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.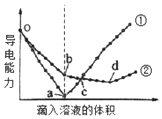 在两份15mL、1mol/L的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
在两份15mL、1mol/L的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
 在两份15mL、1mol/L的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
在两份15mL、1mol/L的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )| A. | o-b段,发生的离子方程式:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | bd段,发生的离子方程式:OH-+H+═H2O | |
| C. | c点,两溶液中阴、阳离子的浓度之和相等 | |
| D. | o-a段加入溶液的体积为20mL,则NaHSO4溶液的浓度为0.75mol/L |
20.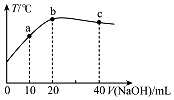 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
 在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )
在一隔热系统中,向20.00mL 0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol.L-1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( )| A. | 若a点溶液呈酸性,此时:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-) | |
| B. | B.从a到b:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | 水的电离程度:b点<c点 | |
| D. | 溶液的pH值:a点<c点<b点 |
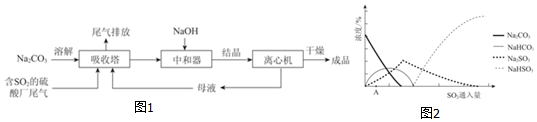
18.二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为 11℃,可用于处理含硫废水.某小组在实验室中探究 ClO2 与 Na2S 的反应.回答下列问题:
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4
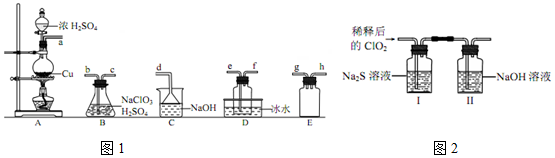
①装置 A 中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的 ClO2,选择图1中的装置,其连接顺序为 a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置 D 的作用是冷凝并收集ClO2.
(2)ClO2 与 Na2S 的反应
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入如图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究 I 中反应的产物.
④ClO2 与 Na2S 反应的离子方程式为8ClO2+5S2-+4H2O=8Cl-+5SO42-+8H+.用于处理含硫废水时,ClO2 相对于Cl2 的优点是ClO2除硫效果彻底,氧化产物硫酸根更稳定、ClO2在水中的溶解度大、剩余的ClO2不会产生二次污染、均被还原为氯离子时,ClO2得到的电子数是氯气的2.5倍(任写一条).
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4

①装置 A 中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的 ClO2,选择图1中的装置,其连接顺序为 a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置 D 的作用是冷凝并收集ClO2.
(2)ClO2 与 Na2S 的反应
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入如图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究 I 中反应的产物.
| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无SO2(或HSO3-或SO32-)生成 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②白色沉淀 | 有SO42-生成 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙内 加入足量稀硝酸酸化的硝酸银溶液 | 有白色沉淀生成 | 有Cl-生成 |