题目内容
13.请回答:(1)乙醇的结构式为
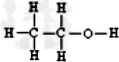 .
.(2)0.3mol B2H6 (g)在O2(g)中燃烧生成固态三氧化二硼和液态水放出649.5KJ热量.用热化学方程式表示B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ•mol-1.
(3)牙齿表面的矿物质成分是羟基磷灰石[Ca5(PO4)3(OH)],含氟牙膏防龋齿是因为牙膏中的氟离子会与羟基磷灰石反应生成更难溶的氟磷灰石[Ca5(PO4)3F],该沉淀转化反应的离子方程式是Ca5(PO4)3OH+F-=Ca5(PO4)3F+OH-.
(4)配平氧化还原反应的离子方程式:
2 MnO4-+5 SO2+2H2O═2Mn2++5SO42-+4H+.
分析 (1)乙醇中含有CH3CH2-和-OH;
(2)0.3molB2H6气体在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,则1molB2H6完全反应放出2165 kJ热量,据此书写热化学反应方程式;
(3)Ca5(PO4)3(OH)生成Ca5(PO4)3F,反应后同时生成OH-;
(4)结合电荷守恒、电子守恒配平方程式.
解答 (1)乙醇中含有CH3CH2-和-OH,结构式为 ,故答案为:
,故答案为: ;
;
(2)0.3molB2H6气体在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,则1molB2H6完全反应放出2165 kJ热量,则该热化学反应方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165 kJ•mol-1 ,
故答案为:B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165 kJ•mol-1 ;
(3)由题意可知反应离子方程式为Ca5(PO4)3OH+F-=Ca5(PO4)3F+OH-,故答案为:Ca5(PO4)3OH+F-=Ca5(PO4)3F+OH-;
(4)反应中Mn元素化合价由+7价降低为+2价,S元素化合价由+4价升高到+6价,反应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
故答案为:2,5,2H2O,2,5,4H+.
点评 本题多角度考查离子方程式、氧化还原反应等知识,侧重学生的分析能力的考查,为高频考点,注意把握物质的性质,难度中等.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
4.我国晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又成丹砂”(注:丹砂即硫化汞).下列说法正确的是( )
| A. | 该过程中仅有物理变化,没有化学变化 | |
| B. | 该过程描述的是一个可逆反应的两个方向 | |
| C. | 该过程设计的反应中包括HgS$\frac{\underline{\;\;△\;\;}}{\;}$Hg+S | |
| D. | 水银有毒,所以生活中绝对不能使用 |
1.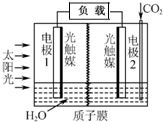 利用人工模拟光合作用合成甲酸的原理为:2CO2+2H2O$→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
利用人工模拟光合作用合成甲酸的原理为:2CO2+2H2O$→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
 利用人工模拟光合作用合成甲酸的原理为:2CO2+2H2O$→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )
利用人工模拟光合作用合成甲酸的原理为:2CO2+2H2O$→_{光触媒}^{太阳能}$ 2HCOOH+O2,装置如图所示,下列说法不正确的是( )| A. | 电子由电极1经过负载流向电极2 | |
| B. | 若将质子膜换成阴离子交换膜,该电池依然能够正常工作 | |
| C. | 电极2的反应式:CO2+2H++2e-=HCOOH | |
| D. | 该装置能将太阳能转化为化学能和电能 |
18.将一定量的SO2通人BaCl2溶液中,无沉淀产生,若再通入a气体,则产生沉淀.下列所通a气体和产生沉淀的离子方程式正确的是( )
| A. | a为H2S,SO2+2H++S2-→3 S↓十2H2O | |
| B. | a为Cl2,Ba2++SO2+2 H2O+Cl2→BaSO3↓+4H++2Cl- | |
| C. | a为NO2,4Ba2++4SO2+5H2O+NO3-→4 BaSO4↓+NH4++6 H+ | |
| D. | a为NH3,Ba2++SO2+2 NH3+2H2O→BaSO4↓+2NH4++2H+ |
2.下列有关物质的性质与其应用不相对应的是( )
| A. | Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 | |
| B. | NH3 能与Cl2 生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏 | |
| C. | NaHCO3 能与碱反应,食品工业用作焙制糕点的膨松剂 | |
| D. | K2FeO4 能与水作用生成Fe(OH)3 胶体和O2,可用于净化自来水并杀菌消毒 |
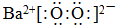 .
.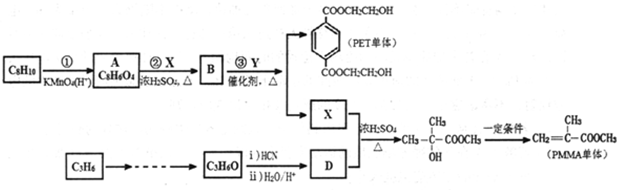
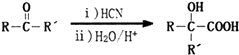
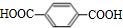 +2CH3OH$→_{△}^{浓硫酸}$
+2CH3OH$→_{△}^{浓硫酸}$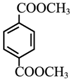 +2H2O.
+2H2O.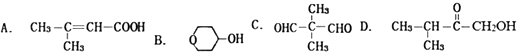
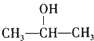 $→_{△}^{O_{2}/Cu}$
$→_{△}^{O_{2}/Cu}$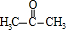 .
.
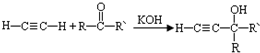
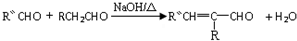 (-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
(-R、-R′、-R″表示可能相同或可能不同的原子或原子团) .
. .
.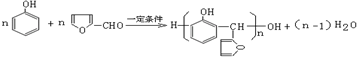 .
.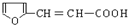 有多种同分异构体,符合下列要求的有9种.
有多种同分异构体,符合下列要求的有9种.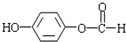 或
或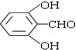 或
或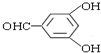 (任写一种).
(任写一种).