题目内容
18.有下列粒子:(1)CH4(2)H3O+(3)N2(4)CO(5)NH4+(6)H2O,其中粒子中质子数和电子数都分别相同的是(1)(3)(4)(6).分析 分子:核外电子数=质子数;阳离子:核外电子数=质子数-电荷数:阴离子核外电子数=质子数+电荷数.
解答 解:(1)CH4质子数为10,电子数为10;
(2)H3O+质子数为11,电子数为10;
(3)N2质子数为14,电子数为14;
(4)CO质子数为14,电子数为14;
(5)NH4+质子数为11,电子数为10;
(6)H2O质子数为10,电子数为10;
故答案为:(1)(3)(4)(6).
点评 本题考查微粒中质子数和电子数的判断,难度不大.要注意质子数与核外电子数的关系.

练习册系列答案
相关题目
8.实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl $\frac{\underline{\;加热\;}}{\;}$NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
| A. | NaNO2是氧化剂,NH4Cl是还原剂 | |
| B. | N2既是氧化产物,又是还原产物 | |
| C. | 氧化剂和还原剂的物质的量之比是1:1 | |
| D. | 每生成1 mol N2时,转移电子的物质的量为6 mol |
9.在一定温度和压强下,1体积A2气体和3体积B2气体恰好化合成2体积的C气体,则C的化学式可能为( )
| A. | AB2 | B. | AB3 | C. | A3B | D. | A2B3 |
6.一定量的CuS和Cu2S的混合物投入一定浓度的足量的HNO3中,收集到体积比为1:1的NO和NO2混合气,向反应后的溶液中加入足量NaOH溶液,产生蓝色沉淀、过滤、洗涤、灼烧,得到12.0g CuO,则上述混合气体在标准状况下的体积可能是( )
| A. | 8.2L | B. | 11.5L | C. | 15.7L | D. | 16.8L |
18.“类推”是学习化学的一种好方法.但是有些“类推”也会由于物质的特性等原因产生错误.下列几种类推结论中正确的是( )
| A. | 金属镁能在CO2中燃烧,则金属钠也能在CO2中燃烧 | |
| B. | 金属钠与水反应产生NaOH和H2,则金属铜与水反应也能产生Cu(OH)2和H2 | |
| C. | Cl2+H2O?HCl+HClO是氧化还原反应,则ICl+H2O?HCl+HIO也是氧化原反应 | |
| D. | CO2与H2O反应生成H2CO3,则SiO2与H2O反应也可以生成H2SiO3 |
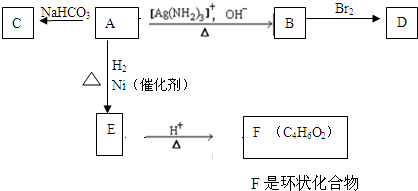
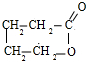 .由E生成F的反应类型是酯化反应.
.由E生成F的反应类型是酯化反应.