题目内容
实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是 .
(2)分离硝基苯和水的混合物的方法是 ;分离硝基苯和苯的方法是 .
(3)实验室制取少量硝基苯:
①实验时应选择 (填“图A”或“图B”)装置;另一装置,存在的2个缺陷是 、 .
②用水浴加热的优点是 .
| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51℃ | 80.1 | 液体 |
| 硝基苯 | 5.7℃ | 210.9℃ | 液体 |
(2)分离硝基苯和水的混合物的方法是
(3)实验室制取少量硝基苯:
①实验时应选择

②用水浴加热的优点是
考点:苯的性质,制备实验方案的设计
专题:实验题,有机物的化学性质及推断
分析:(1)根据浓硫酸与其它液体混合时原则:把浓硫酸加到其它溶液中;
(2)硝基苯和水是互不相溶的;硝基苯和苯互溶,沸点相差较大;
(3))①水浴加热时,试管底部与烧杯底部接触会使温度过高;苯和硝酸易挥发;
②根据水浴加热的特点分析.
(2)硝基苯和水是互不相溶的;硝基苯和苯互溶,沸点相差较大;
(3))①水浴加热时,试管底部与烧杯底部接触会使温度过高;苯和硝酸易挥发;
②根据水浴加热的特点分析.
解答:
解:(1)试剂的混合:把浓硫酸缓缓注入到浓硝酸中并及时搅拌冷却,最后逐滴加入苯,边加边振荡,使混酸与苯混合均匀,
故答案为:将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌;
(2)硝基苯和水互不相溶,可用分液的方法分离,硝基苯和苯互溶,沸点相差较大,可考虑用蒸馏的方法分离,故答案为:分液;蒸馏;
(3)①水浴加热时,试管底部与烧杯底部接触会使温度过高;苯和硝酸易挥发,即浪费原料,又会污染环境,所以要有冷凝回流装置,所以应该选用图B;
故答案为:图B;没有冷凝回流装置;试管底部与烧杯底部接触;
②水浴加热可以使反应物受热均匀,并且温度容易控制,
故答案为:使反应体系受热均匀,容易控制温度.
故答案为:将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌;
(2)硝基苯和水互不相溶,可用分液的方法分离,硝基苯和苯互溶,沸点相差较大,可考虑用蒸馏的方法分离,故答案为:分液;蒸馏;
(3)①水浴加热时,试管底部与烧杯底部接触会使温度过高;苯和硝酸易挥发,即浪费原料,又会污染环境,所以要有冷凝回流装置,所以应该选用图B;
故答案为:图B;没有冷凝回流装置;试管底部与烧杯底部接触;
②水浴加热可以使反应物受热均匀,并且温度容易控制,
故答案为:使反应体系受热均匀,容易控制温度.
点评:本题考查了实验室制备硝基苯的方法,注意根据表格中的数据分析判断,结合物质的性质分析装置图,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有机物的系统命名中正确的是( )
| A、CH3CH(C2H5)CH3 2-乙基丙烷 |
| B、CH3CH2CH2CH2OH 1-丁醇 |
C、 间二甲苯 间二甲苯 |
D、 2-甲基-2-丙烯 2-甲基-2-丙烯 |
氢化钙(CaH2中H为-1价)可作为生氢剂,反应的化学方程式为CaH2+2H2O═Ca(OH)2+2H2↑.下列说法错误的是( )
| A、标准状况下生成1mol H2时转移2NA个电子 |
| B、CaH2是还原剂,H2O是氧化剂 |
| C、H2既是氧化产物又是还原产物 |
| D、氧化产物和还原产物的质量比是1:1 |
用NA表示阿伏加德常数的值,下列说法正确的是( )
| A、1mol NaHSO4晶体中含有的离子总数为3NA |
| B、12.4g白磷(分子式为P4)中含有的P-P键为0.6 NA |
| C、28g C2H4 和C4 H8混合气体中含有的原子总数为9NA |
| D、200mL 10mol/L的浓硝酸与足量的铜片反应,生成的NO2分子数目为NA |
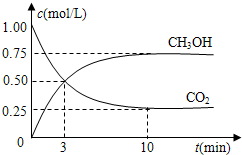 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图. (1)写出相对分子质量为128的烃的分子式:
(1)写出相对分子质量为128的烃的分子式: