题目内容
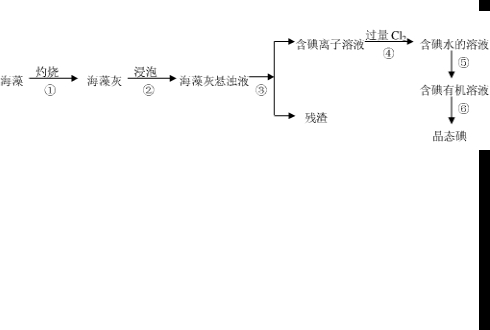
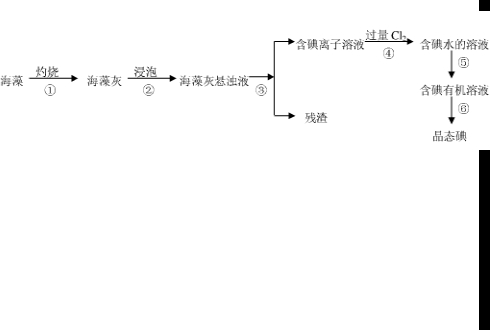
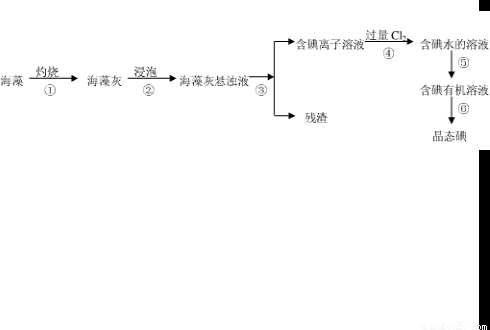
 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下:
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下: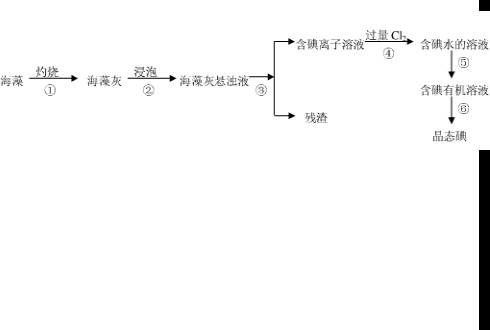
(1)指出上述提取碘的过程中有关实验操作的名称:
步骤③
过滤
过滤
,步骤⑤萃取
萃取
.(2)步骤④也可以先在滤液中滴入几滴稀硫酸,再加入足量H2O2,此时发生反应的离子方程式为:
H2O2+2I-+2H+=I2+2H2O
H2O2+2I-+2H+=I2+2H2O
.(3)提取碘的过程中,可供选择的有机试剂是
CD
CD
.(填编号)A.酒精 B.醋酸 C.四氯化碳 D.苯
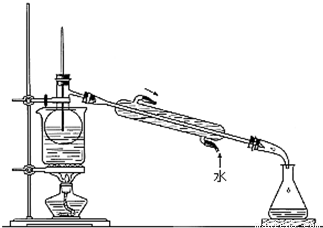
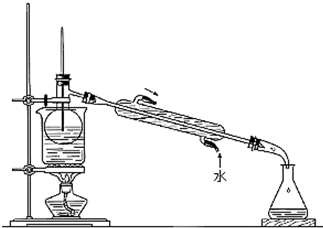
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出右图实验装置中存在的错误之处并改正:
温度计水银球的位置错误,应与蒸馏烧瓶的支管口相平
温度计水银球的位置错误,应与蒸馏烧瓶的支管口相平
.(5)进行上述蒸馏操作时,使用水浴的原因是
试剂受热均匀
试剂受热均匀
.分析:(1)分离固体和液体用过滤;用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来用萃取;
(2)双氧水(H2O2)可氧化碘离子;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;
(4)温度计水银球应与烧瓶支管口相平;
(5)水浴加热试管内试剂受热比较均匀.
(2)双氧水(H2O2)可氧化碘离子;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;
(4)温度计水银球应与烧瓶支管口相平;
(5)水浴加热试管内试剂受热比较均匀.
解答:解:(1)分离固体和液体用过滤;用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来用萃取,故答案为:过滤;萃取;
(2)在酸性条件下双氧水(H2O2)可氧化碘离子,故答案为:H2O2+2I-+2H+=I2+2H2O;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,故可用四氯化碳或苯,故选CD;
(4)温度计水银球应与烧瓶支管口相平,故答案为:温度计水银球的位置错误,应与蒸馏烧瓶的支管口相平;
(5)水浴加热试管内试剂受热比较均匀,故答案为:试剂受热均匀.
(2)在酸性条件下双氧水(H2O2)可氧化碘离子,故答案为:H2O2+2I-+2H+=I2+2H2O;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,故可用四氯化碳或苯,故选CD;
(4)温度计水银球应与烧瓶支管口相平,故答案为:温度计水银球的位置错误,应与蒸馏烧瓶的支管口相平;
(5)水浴加热试管内试剂受热比较均匀,故答案为:试剂受热均匀.
点评:本题考查物质的分离和提纯,学习中注意掌握过滤、萃取、蒸馏等操作.

练习册系列答案
相关题目

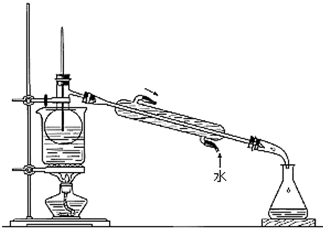 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下:
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下: