题目内容
12.下列关于物质用途的叙述中不正确的是( )| A. | Na2O2可用作呼吸面具中的供氧剂 | |
| B. | 浓硫酸在常温下不能与铜片反应放出二氧化硫气体 | |
| C. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| D. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 |
分析 A.Na2O2能和CO2、H2O反应生成O2;
B.常温下,浓硫酸和Cu不反应,加热条件下反应生成二氧化硫;
C.Al(OH)3具有两性,能和酸反应生成盐和水;
D.Fe3O4俗称磁铁且为黑色固体、Fe2O3俗称赤铁且为红棕色固体.
解答 解:A.Na2O2能和CO2、H2O反应生成O2,过氧化钠能吸收人呼出的CO2、H2O且制造氧气,实现废物利用,所以Na2O2可用作呼吸面具中的供氧剂,故A正确;
B.常温下,浓硫酸和Cu不反应,加热条件下反应生成二氧化硫,所以浓硫酸在常温下不能与铜片反应放出二氧化硫气体,故B正确;
C.Al(OH)3具有两性,能和酸反应生成盐和水,且氢氧化铝腐蚀性较弱,所以Al(OH)3可作治疗胃酸过多的一种药剂,故C正确;
D.Fe3O4俗称磁铁且为黑色固体、Fe2O3俗称赤铁且为红棕色固体,Fe2O3可用于作油漆、红色涂料,故D错误;
故选D.
点评 本题考查元素化合物知识,为高频考点,明确常见元素化合物性质是解本题关键,性质决定用途、用途体现性质,NaHCO3也可以治疗胃酸过多,知道铁的氧化物颜色,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
2.在溶液中能大量共存的离子组是( )
| A. | K+、Fe3+、SCN-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、CO32- | D. | Na+、Cu2+、Cl-、SO42- |
3.二氧化硫能够使高锰酸钾溶液褪色,表现了二氧化硫的( )
| A. | 酸性 | B. | 氧化性 | C. | 还原性 | D. | 漂白性 |
20.在高炉中,还原氧化铁的物质是( )
| A. | 二氧化碳 | B. | 铁矿石 | C. | 石灰石 | D. | 一氧化碳 |
7.下列关于性质或用途的说法正确的是( )
| A. | 某物质灼烧时,火焰颜色为黄色,则该物质为金属钠 | |
| B. | 工业制造镁粉是将镁蒸气放在氮气中冷却 | |
| C. | 钠的化学性质很活泼,所以在自然界中只能是以游离态的形式存在 | |
| D. | 钠钾合金可以用于快中子反应堆作热交换剂 |
17.某非金属元素R的氢化物及其氧化物、盐之间具有如下转化关系(部分产物省略):氢化物$\stackrel{氧气}{→}$B$\stackrel{Na_{2}O_{2}}{→}$ C,下列判断中正确的是( )
| A. | 若R是硫元素、则C是Na2SO3 | B. | 若R是硅元素、则C是Na2Si03 | ||
| C. | 若R是碳元素、则C是Na2CO3 | D. | 若R是氯元素、则C是NaCl |
4.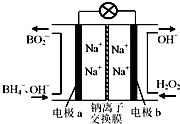 以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
 以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A. | 电极a采用MnO2,MnO2既作电极材料又有催化作用 | |
| B. | 电池放电时Na+从a极区移向b极区 | |
| C. | 每消耗3mol H2O2,转移的电子为3mol | |
| D. | 该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
1.下列实验操作正确的是( )
| A. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| B. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,则该溶液一定是碳酸盐溶液 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 中和热测定实验中,要将酸和碱迅速混合,以防热量散失 |
20.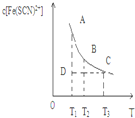 FeCl3与KSCN混合时存在下列平衡:Fe3++SCN-?[Fe( SCN)]2+.已知平衡时,物质的量浓度c[Fe(SCN)]2+与温度T的关系如图,则下列说法正确的是( )
FeCl3与KSCN混合时存在下列平衡:Fe3++SCN-?[Fe( SCN)]2+.已知平衡时,物质的量浓度c[Fe(SCN)]2+与温度T的关系如图,则下列说法正确的是( )
 FeCl3与KSCN混合时存在下列平衡:Fe3++SCN-?[Fe( SCN)]2+.已知平衡时,物质的量浓度c[Fe(SCN)]2+与温度T的关系如图,则下列说法正确的是( )
FeCl3与KSCN混合时存在下列平衡:Fe3++SCN-?[Fe( SCN)]2+.已知平衡时,物质的量浓度c[Fe(SCN)]2+与温度T的关系如图,则下列说法正确的是( )| A. | FeCl3与KSCN反应的热化学反应方程式为:Fe3++SCN-?[Fe( SCN)]2+△H>0 | |
| B. | 温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1>K2 | |
| C. | 反应处于D点时,一定有V正>V逆 | |
| D. | T2温度下,向B点溶液中加入FeCl3 固体,平衡状态会从 B点变到A点 |