题目内容
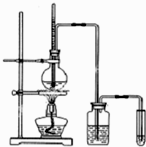 下面是实验室制乙烯并检验其性质的装置图,请回答:
下面是实验室制乙烯并检验其性质的装置图,请回答:(1)写出圆底烧瓶中反应的方程式
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
(3)为了检验乙烯的生成,试管中应盛放
(4)洗瓶中盛放的试剂为
考点:乙烯的实验室制法,乙烯的化学性质
专题:
分析:(1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是170℃;
(2)碳和热的浓硫酸反应生成二氧化碳、二氧化硫和水;
(3)乙烯被高锰酸钾氧化;
(4)二氧化硫与高锰酸钾溶液反应.
(2)碳和热的浓硫酸反应生成二氧化碳、二氧化硫和水;
(3)乙烯被高锰酸钾氧化;
(4)二氧化硫与高锰酸钾溶液反应.
解答:
解:(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应为CH3CH2OH
CH2=CH2↑+H2O,
故答案为:CH3CH2OH
CH2=CH2↑+H2O; 消去反应;
(2)乙醇被浓硫酸氧化成碳,碳被浓硫酸氧化成二氧化碳,硫酸被还原成二氧化硫,化学方程式:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;
(3)高锰酸钾具有强氧化性,乙烯含有不饱和键,C=C双键,能被高锰酸钾溶液氧化,C=C双键,能卤素单质发生加成反应,乙烯易和溴加成生成1,2-二溴乙烷,
故答案为:高锰酸钾溶液(或溴的四氯化碳溶液); 溶液褪色;
(4)二氧化硫与高锰酸钾溶液反应,所以用NaOH溶液除去SO2,CO2,SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH=Na2CO3+H2O,
故答案为:氢氧化钠溶液;吸收SO2和CO2.
| 浓H2SO4 |
| 170℃ |
故答案为:CH3CH2OH
| 浓H2SO4 |
| 170℃ |
(2)乙醇被浓硫酸氧化成碳,碳被浓硫酸氧化成二氧化碳,硫酸被还原成二氧化硫,化学方程式:C+2H2SO4(浓)
| ||
故答案为:C+2H2SO4(浓)
| ||
(3)高锰酸钾具有强氧化性,乙烯含有不饱和键,C=C双键,能被高锰酸钾溶液氧化,C=C双键,能卤素单质发生加成反应,乙烯易和溴加成生成1,2-二溴乙烷,
故答案为:高锰酸钾溶液(或溴的四氯化碳溶液); 溶液褪色;
(4)二氧化硫与高锰酸钾溶液反应,所以用NaOH溶液除去SO2,CO2,SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH=Na2CO3+H2O,
故答案为:氢氧化钠溶液;吸收SO2和CO2.
点评:本题考查乙烯的实验室制法以及乙烯的性质,注意常见有机物的制备知识的积累,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
向10mL0.1mol?L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是( )
| A、x=10时,溶液中有NH4+、Al3+、SO42-,且c( NH4+)>c(Al3+) |
| B、x=15时,溶液中有NH4+、SO42-,且c(NH4+)<2c(SO42-) |
| C、x=20时,溶液中有NH4+、Al3+、OH-,且c(OH-)<c(Al3+) |
| D、x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)=c(Ba2+) |
25℃时,水的电离达到平衡,下列叙述正确的是( )
| A、向水中加入少量NaOH,平衡逆向移动,新平衡时c(OH-)降低 |
| B、向水中加入少量NH4Cl,平衡正向移动,新平衡时c(OH-)降低 |
| C、pH=5的醋酸和pH=9的氨水中由水电离出的c(OH-)不相等 |
| D、将水加热,Kw增大,pH不变 |
体积相同、pH相同的盐酸和醋酸溶液,与NaOH溶液中和时两者消耗NaOH的物质的量( )
| A、盐酸多 | B、醋酸多 |
| C、二者相同 | D、无法比较 |
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1,则氢气的标准燃烧热为-241.8 kJ?mol-1 |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.65 kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1 |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
下列变化中,△S<0的是( )
| A、氯化钠溶于水 |
| B、NH3(g)与HCl(g)反应生成NH4Cl(s) |
| C、干冰(CO2)的升华 |
| D、CaCO3(s)分解为CaO(s)和CO2(g) |
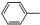 外,不再含其他环状结构,还含有3个-CH3、1个-CH2-、1个
外,不再含其他环状结构,还含有3个-CH3、1个-CH2-、1个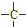 ,它可能的结构有( )
,它可能的结构有( )