题目内容
为我国的化学工业作出重大贡献的科学家是( )
| A、邓稼先 | B、侯德榜 | C、李四光 | D、华罗庚 |
分析:A.根据邓稼先的研究成果判断;
B、根据侯德榜在化学工业上的贡献判断;
C.根据李四光的研究成果判断;
D.根据华罗庚的研究成果判断.
B、根据侯德榜在化学工业上的贡献判断;
C.根据李四光的研究成果判断;
D.根据华罗庚的研究成果判断.
解答:解:A.邓稼先是中国著名核物理学家,是我国核武器理论研究工作的奠基者之一,故A错误;
B.侯德榜发明了联合制碱法,亦称侯氏制碱法,改进了制碱工艺,在制得纯碱的同时,还能生产氮肥,故B正确;
C.李四光是一位地质学家,于本世纪20年代创立了地质力学,为地质理论作出了巨大贡献,故C错误;
D.华罗庚是一位数学家,华罗庚的研究领域遍及数论、代数、矩阵几何学,典型群,多个复变数函数论、应用数学等,故D错误,
故选B.
B.侯德榜发明了联合制碱法,亦称侯氏制碱法,改进了制碱工艺,在制得纯碱的同时,还能生产氮肥,故B正确;
C.李四光是一位地质学家,于本世纪20年代创立了地质力学,为地质理论作出了巨大贡献,故C错误;
D.华罗庚是一位数学家,华罗庚的研究领域遍及数论、代数、矩阵几何学,典型群,多个复变数函数论、应用数学等,故D错误,
故选B.
点评:了解化学的发展史,有利于激发学生学习化学的兴趣,培养社会责任感.

练习册系列答案
相关题目
 和
和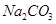 的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。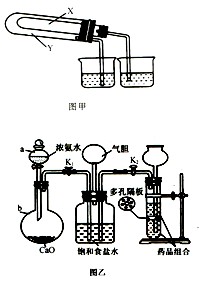
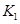 、
、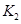 的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。