题目内容
4.用NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 1mol铁与足量的氯气完全反应转移的电子数为2NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 标准状况下,1molCO2、CO的混合气中含有的碳原子数为NA | |
| D. | 1L1mol•L-1CuCl2溶液中含有的氯离子数为NA |
分析 A、铁和氯气反应后变为+3价;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、二氧化碳和CO中均含1个碳原子;
D、求出氯化铜的物质的量,然后根据氯化铜中含2个氯离子来分析.
解答 解:A、铁和氯气反应后变为+3价,故1mol铁反应转移3NA个电子,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2LHCl的物质的量小于0.5mol,则分子个数小于0.5NA个,故B错误;
C、二氧化碳和CO中均含1个碳原子,故1mol二氧化碳和CO中含有的碳原子的物质的量为1mol,个数为NA个,故C正确;
D、溶液中氯化铜的物质的量n=CV=1mol/L×1L=1mol,而氯化铜中含2个氯离子,故1mol氯化铜中含2NA个氯离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp3杂化 | |
| C. | 氯化硼分子属极性分子 | |
| D. | 氯化硼遇水蒸气会产生白雾 |
15.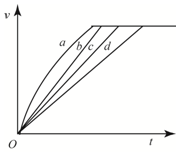 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )| 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
| A. | 第1组实验中盐酸的浓度大于2.5mol•L-1 | |
| B. | 第2组实验中盐酸的浓度大于2.5mol•L-1 | |
| C. | 第3组实验的反应温度低于30℃ | |
| D. | 第4组实验的反应速度最慢 |
12.关于金属元素在自然界存在的情况的叙述中,正确的是( )
| A. | 金属元素仅存在于矿物中 | |
| B. | 金属元素存在于矿物和动物体內,但植物体內不含 | |
| C. | 少数金属元素以游离态存在,大多数金属元素以化合态存在 | |
| D. | 金属元素仅存在矿物中,动物和植物体內也不存在金属元素 |
19.有关下列图象说法错误的是( )
| A. | 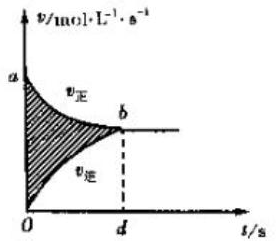 图阴影部分面积表示反应物浓度的净减少量M | |
| B. | 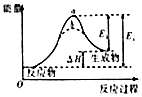 图虚线b表示反应加入催化剂后能量变化曲线 | |
| C. | 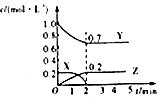 图为可逆反应的浓度一时间图,化学方程式为2X(g)+3Y(g)?2Z(g) | |
| D. |  图对应于反应H2(g)+CO2(g)?H2O(g)+CO(g),曲线I变为曲线II和曲线III改变的条件分别是加入催化剂和将容器的体积快速压缩为原来的$\frac{2}{3}$ |
16.蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成.现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,得到沉淀X和滤液Y.下列叙述正确的是( )
| A. | 沉淀X的成分是SiO2、Fe2O3 | |
| B. | 在溶液Y中加入过量的氨水,过滤得到的沉淀是Al(OH)3、Fe(OH)3和Mg(OH)2 | |
| C. | 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ | |
| D. | 从蛇纹石组成看,其成皆是碱性氧化物 |
13.下列有关物质性质的应用错误的是( )
| A. | 硅酸盐可用于制作光导纤维 | |
| B. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 | |
| C. | 明矾溶于水后会产生Al(OH)3胶体,可作为净水剂 | |
| D. | 液氨挥发时会吸收大量的热,可作为制冷剂 |