题目内容
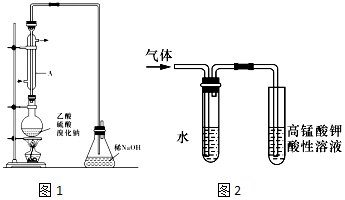
12.溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式为:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.I.实际通常是用溴化钠与一定浓度的硫酸和乙醇反应.某课外小组欲在实验室制备溴乙烷的装置如图1,实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应.
请问答下列问题.
(1)装置A的作用是冷凝回流.
(2)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是Br2.
(3)反应结束后,得到的粗产品呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的a(填写正确选项的字母).
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是分液漏斗(填仪器名称).
II.溴乙烷的性质实验
(4)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是.通常采用的方法是取少量溴乙烷,然后④①③②(按实验的操作顺序选填下列序号).
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
(5)溴乙烷与NaOH乙醇溶液共热可产生乙烯气体.在进行该实验时,把生成的气体通过图2所示的装置.用该装置进行实验的目的是检验乙烯的生成,图2中右侧试管中的现象是酸性高锰酸钾溶液褪色;左侧试管中水的作用是除去乙醇等杂质干扰.
分析 I.(1)长玻璃导管的作用是冷凝回流;
(2)浓硫酸具有氧化性,可以将还原性的溴离子氧化为溴单质;
(3)溴单质溶解在有机物中显示棕黄色,溴单质可以和氢氧化钠发生反应;实现互不相溶液体的分离采用分液漏斗来分液;
(4)检验溴乙烷中含有溴元素一定要将之转化为溴离子,根据溴离子可以和银离子反应生成淡黄色不溶于硝酸的沉淀来检验
II.(5)在加热条件下,溴乙烷和氢氧化钠的醇溶液发生消去反应生成乙烯和HBr,HBr、乙醇极易溶于水,乙烯不易溶于水,乙烯能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.
解答 解:I.(1)实验时,长玻璃导管的作用是冷凝回流,可以获得要制取的有机物,
故答案为:冷凝回流;
(2)浓硫酸具有氧化性,可以将还原性的溴离子氧化为溴单质,得到的红棕色气体为溴蒸气,浓硫酸自身被还原为二氧化硫,
故答案为:Br2;
(3)溴单质溶解在有机物中显示棕黄色,为了除去粗产品中的杂质溴单质,溴在乙醇中溶解度不大,故不选;CCl4能溶解溴乙烷和溴,故不选,可以用氢氧化钠来与之发生反应生成的溶液和溴乙烷互不相溶,实现溴乙烷和氯化钠、次氯酸钠水溶液的分离可以采用分液法,用分液漏斗来分液,
故答案为:a;分液漏斗;
(4)溴乙烷为非电解质,不能电离出Br-,检验溴乙烷中含有溴元素一定要将之转化为溴离子,可以采用卤代烃的水解方法,即加入氢氧化钠即可,在溴离子可以和银离子反应生成淡黄色不溶于硝酸的沉淀溴化银来检验,可以加入硝酸酸化的硝酸银,所以实验的操作顺序为④①③②,
故答案为:溴乙烷为非电解质,不能电离出Br-,不能与硝酸银溶液反应生成沉淀;④①③②;
(5)在加热条件下,溴乙烷和氢氧化钠的醇溶液发生消去反应生成乙烯和HBr,HBr、乙醇极易溶于水,乙醇和HBr都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烯不易溶于水,乙烯能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以看到的现象是:右边试管中酸性高锰酸钾溶液褪色,左边试管中水的作用是除去乙醇等杂质的干扰,
故答案为:酸性高锰酸钾溶液褪色;除去乙醇等杂质干扰.
点评 本题考查物质制备实验,为高频考点,考查学生实验分析的能力,明确实验原理及基本操作步骤是解本题关键,知道卤代烃中卤元素检验方法及实验现象,易错点是(5)中乙醇能被酸性高锰酸钾溶液氧化,题目难度中等.

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案| A. | Fe2+ | B. | NH4+ | C. | Al3+ | D. | Fe3+ |
| A. | 容器内压强不随时间变化 | |
| B. | 容器内各物质的浓度不随时间变化 | |
| C. | 容器内各物质X、Y、Z的浓度之比为1:1:2 | |
| D. | 单位时间内消耗0.1 molX,同时生成0.2 molZ |
| A. | Na+、NO3- | B. | S2-、AlO2- | C. | Al3+、Fe3+ | D. | MnO4-、NH4+ |
| A. | 肯定不含 I- | B. | 肯定不含 SO42- | C. | 可能含有 SO32- | D. | 肯定含有 NH4+ |
| A. | 一定条件下,用秸秆可制得葡萄糖和酒精 | |
| B. | 铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁的稳定 | |
| C. | 氧气被用作火箭的燃料,利用了氧气的可燃性 | |
| D. | 稀有气体充入霓虹灯,利用了稀有气体通电时发出不同颜色的光的化学性质 |
N2(g)+3H2(g)?2NH3(g)△H=一92.4KJ•mol-1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将逆向(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为$\frac{a}{100V}$mol•L-1.(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]:
CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3.反应中CO2( g)的物质的量随时间变化如表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为76.53(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是B(填图甲中的“A”或“B”).
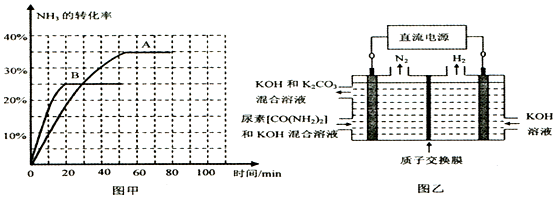
⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2-6e-+8OH-=CO32-+N2↑+6H2O,若两极共收集到气体22.4L(标况),则消耗的尿素为15g(忽略气体的溶解).
实验一:
| 实验A | 实验B | |
| 操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液. | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水. |
| 现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)