题目内容
4.用CH 3CH 2CH 2OH 制取聚丙烯可能遇到的反应类型有( )| A. | 取代 | B. | 消去 | C. | 加聚 | D. | 酯化 |
分析 可采用逆向合成分析法: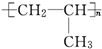 ←CH2=CH-CH3←CH3CH2CH2OH,以此解答该题.
←CH2=CH-CH3←CH3CH2CH2OH,以此解答该题.
解答 解:用CH 3CH 2CH 2OH 制取聚丙烯的反应应是,先用CH 3CH 2CH 2OH消去制取除CH 3CH=CH 2,然后在加聚生成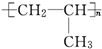 .
.
故选BC.
点评 本题考查有机物的合成,把握官能团的变化及性质为解答的关键,侧重有机物性质及化学反应的考查,明确合成发生的反应类型为解答的关键,题目难度不大.

练习册系列答案
相关题目
14.将固体NH4Br置于密闭容器中,在某温度下,发生下列反应:NH4Br(s)═NH3(g)+HBr(g),2HBr(g)?Br2(g)+H2(g).2min时,测知H2的浓度为0.5mol•L-1,HBr的浓度为4mol•L-1,若上述反应速率用v(NH3)表示,下列速率正确的是( )
| A. | 0.5mol•L-1•min-1 | B. | 2.5mol•L-1•min-1 | ||
| C. | 2mol•L-1•min-1 | D. | 5mol•L-1•min-1 |
12.X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如表
(1)Q元素基态原子的电子排布式是1s22s22p63s23p63d64s2,Y原子的电子排布图是 .
.
(2)比较Y元素与氧元素的第一电离能N>O;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是CS2,分子中的 键和π键数目之比为1:1.
键和π键数目之比为1:1.
(3)写出实验室制备M单质的离子方程式MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是HF>HCl,其原因是因为元素非金属性F>Cl,所以HF稳定;
沸点高的是HF>HCl,其原因是因为HF分子之间存在氢键,所以HF沸点高.
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
 .
.(2)比较Y元素与氧元素的第一电离能N>O;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是CS2,分子中的
 键和π键数目之比为1:1.
键和π键数目之比为1:1.(3)写出实验室制备M单质的离子方程式MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是HF>HCl,其原因是因为元素非金属性F>Cl,所以HF稳定;
沸点高的是HF>HCl,其原因是因为HF分子之间存在氢键,所以HF沸点高.
9.A、B、C、D、E均为元素周期表中短周期元素,其原子序数依次递增.请结合下表信息回答问题:
(1)元素B和E形成的化合物的电子式为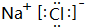 ,该化合物含有离子键(填“离子键”或“共价键”).
,该化合物含有离子键(填“离子键”或“共价键”).
(2)B的单质在A的单质中燃烧的化学方程式为2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2
(3)元素D、E的最高价氧化物对应的水化物的酸性HClO4 大于H2SO4(填化学式).
(4)请举出C单质的一种用途硅芯片、太阳能电池板等.
| 元素 | 有关信息 |
| A | 位于第二周期第 VIA族 |
| B | 焰色反应呈黄色 |
| C | 无机非金属材料的主角 |
| D | 与A同主族 |
| E | 原子序数比D多1 |
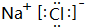 ,该化合物含有离子键(填“离子键”或“共价键”).
,该化合物含有离子键(填“离子键”或“共价键”).(2)B的单质在A的单质中燃烧的化学方程式为2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2
(3)元素D、E的最高价氧化物对应的水化物的酸性HClO4 大于H2SO4(填化学式).
(4)请举出C单质的一种用途硅芯片、太阳能电池板等.
16.下列有关说法正确的是( )
| A. | 硫酸工业中二氧化硫的催化氧化,不采用高压是因为压强对SO2转化率无影响 | |
| B. | 同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | |
| C. | 3C(s)+CaO(s)═CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| D. | 合成氨时,其他条件不变升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
13.在酸性溶液中,下列各组离子能大量共存的是( )
| A. | Al3+ Mg2+ Cl- NO3- | B. | Na+ Fe3+ Al3+ OH- | ||
| C. | K+ NH4+ | D. | Na+ K+ CH3COO- |
14.下列各项表述正确的是( )
| A. | 已知H2燃烧热△H为-285.8kJ/mol,则:2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | |
| B. | 已知稀盐酸与NaOH稀溶液反应的中和热△H为-57.3kJ/mol,则:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l)△H=-57.3kJ/mol | |
| C. | 电解稀硫酸可能发生反应:Cu+H2SO4$\frac{\underline{\;电解\;}}{\;}$CuSO4+H2↑ | |
| D. | 以石墨为电极电解MgCl2溶液的总离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- |
 三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到.
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到.