题目内容
4.质量分数为36.5%,密度为1.19g/mL的盐酸的物质的量浓度为11.9mol/L,取其10mL稀释至100mL,则稀释后的溶液的物质的量浓度为1.19mol/L.分析 依据c=$\frac{1000ρω}{M}$计算浓盐酸的物质的量浓度,依据溶液稀释过程 中溶质的物质的量不变计算稀释后溶液的物质的量浓度,据此解答.
解答 解:质量分数为36.5%,密度为1.19g/mL的盐酸的物质的量浓度为:$\frac{1000×1.19×36.5%}{36.5}$=11.9mol/L,设稀释后溶液浓度为c′,则依据溶液稀释过程 中溶质的物质的量不变得:11.9mol/L×10mL=c′×100mL,解得c′=1.19mol/L;
故答案为:11.9; 1.19.
点评 本题考查了物质的量浓度有个计算,明确物质的量浓度与质量百分数浓度之间换算,熟悉溶液稀释过程中溶质的物质的量不变规律即可解答,题目难度不大.

练习册系列答案
相关题目
16.下列说法错误的是( )
| A. | C2H4既能使溴水褪色,也能使酸性KMnO4溶液褪色 | |
| B. | 蔗糖和葡萄糖属于同系物 | |
| C. | 用碳酸钠溶液可以区别出乙酸、乙醇和苯三种液体 | |
| D. | 苯乙烯的所有原子都可能在同一平面上 |
17.向溶液中加入新物质时,其导电性(I)符合图变化趋势的实验操作是( )
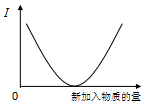

| A. | 乙酸溶液中通入氨气至过量 | B. | 石灰水中通入CO2至过量 | ||
| C. | 亚硫酸中通入氯气至过量 | D. | 氨水中通入氯化氢气体 |
12.某溶液中含有大量的Cl-、CO32-、SO42-等三种阴离子.如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加HNO3溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液.
①滴加HNO3溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液.
| A. | ①④②③ | B. | ④②①③ | C. | ③②①④ | D. | ④②③②① |
19.下列有关Na2CO3和NaHCO3的叙述中,正确的是( )
| A. | 受热时,NaHCO3比Na2CO3容易分解 | |
| B. | NaHCO3俗名苏打,Na2CO3俗名纯碱 | |
| C. | NaHCO3溶液显酸性,Na2CO3溶液显碱性 | |
| D. | NaHCO3和Na2CO3各1mol分别与过量盐酸反应,产生CO2的质量不同 |
9.某气体样品质量是12.8g,标况下的体积4.48L,该气体的摩尔质量为( )
| A. | 28.4 | B. | 28.4 g/mol | C. | 64 | D. | 64 g/mol |
16.如图,CPAE是蜂胶的主要活性成分,也可由咖啡酸合成.下列说法不正确的是( )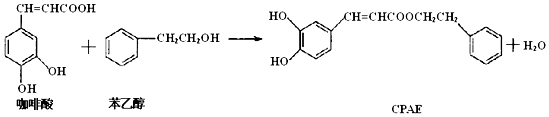

| A. | 咖啡酸分子中所有碳原子可能处在同一个平面上 | |
| B. | 1 mol CPAE与足量的溴水反应,最多消耗3molBr2 | |
| C. | 1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2 | |
| D. | 1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH |
13.下列所得溶液的物质的量浓度等于 0.1mol•L-1 的是( )
| A. | 将 0.1 mol 氨充分溶解在 1 L 水中 | |
| B. | 将 10 g 质量分数为 98%的硫酸与 990 g 水混合 | |
| C. | 将 8 g 三氧化硫溶于水并配成 1 L 溶液 | |
| D. | 将 0.1 mol 氧化钠溶于水并配成 1L 溶液 |
14.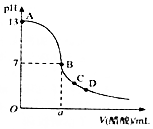 298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )
298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )
 298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )
298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )| A. | a<20 | |
| B. | C点溶液中:c(CH3COO-)+c(CH3COOH)=c(Na+) | |
| C. | A、B、C、D四点水的电离程度大小顺序为:D>B>C>A | |
| D. | 醋酸的电离平衡常数Ka=2.0×10-7/(0.la-2) |