题目内容
15.同温同压下,KMnO4、KClO3、H2O2分解产生相同体积的氧气,三个反应中转移的电子数之比为( )| A. | 1:1:l | B. | 1:1:2 | C. | 2:2:1 | D. | 4:3:2 |
分析 加热高锰酸钾的方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,转移电子是4mol,氯酸钾分解反应的方程式为2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑,转移电子是12mol,2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,转移电子是2mol,根据转移电子的数目和获得氧气的量进行计算.
解答 解:加热高锰酸钾的方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,转移电子是4mol,氯酸钾分解反应的方程式为2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑,转移电子是12mol,2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,转移电子是2mol,当获得氧气常温常压下相同体积时,假设是1mol时,转移电子数分别是4mol、4mol、2mol,所以所转移的电子数目之比是2:2:1.
故选C.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重电子转移计算及分析能力的考查,题目难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
5.表中有三组物质,每组都有一种物质与其他三种物质属于不同类别.请选出该物质,填在表相应的空格内.
| 序号 | 物质 | 被选出的 |
| (1) | O2、H2、C、N2 | C |
| (2) | Fe、Na、Al、Si | Si |
| (3) | NO、CO2、SO2、Fe3O4 | Fe3O4 |
6.化学与生活、社会发展息息相关,下列有关说法不正确的是( )
| A. | 14C可用于文物的年代的鉴定,12C和14C互为同位素 | |
| B. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| C. | 在元素周期表的金属和非金属分界线附近寻找半导体材料 | |
| D. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 |
3.设NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 0.5mol/L亚硫酸钠溶液中含有的SO32-的物质的量为0.5mol | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 过量铜片与100mL18mol/L的浓硫酸反应,转移的电子数为1.8NA |
20.肼(N2H4)-空气燃料电池以KOH溶液为电解质溶液,装置如图所示.下列有关叙述正确的是( )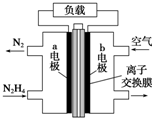

| A. | 放电时,电流从b极经过负载流向a极 | |
| B. | b极发生氧化反应 | |
| C. | a极的反应式为N2H4+4OH--4e-=N2+4H2O | |
| D. | 电池中的离子交换膜需选用阳离子交换膜 |
7.PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOX、O3、CH2=CH-CHO,HCOOH,CH3COOONO2(PAN)等二次污染物.下列说法正确的是( )
| A. | N2O结构式可表示为N=N=O | |
| B. | O3分子呈直线形 | |
| C. | CH2=CH-CHO分子中碳原子均采用sp2杂化 | |
| D. | 相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子 |
4.“化学-我们的生活、我们的未来”.下列有关知识叙述正确的是( )
| A. | Na+、Fe3+是人体所需微量元素 | B. | 苯酚不能用于杀菌消毒 | ||
| C. | 氢气是未来的一种理想燃料 | D. | 乙醇是不可再生的生物质能源 |
5.下列说法正确的是( )
| A. | 沸点由低到高的顺序为:CH3CH2CH3<CH3(CH2)2CH3<(CH3)3CH | |
| B. | 工业上合成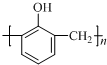 的单体为甲醛和苯酚( 的单体为甲醛和苯酚(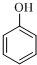 ) ) | |
| C. | 相同质量的乙烯和乙酸完全燃烧时,消耗氧气的量相同 | |
| D. | 某烷烃可以命名为2,3,3-三甲基-4-乙基戊烷 |