题目内容
7.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温常压下,1 L 1 mol•L-1的BaCl2溶液中有NA个Cl- | |
| B. | 1 mol Fe被完全氧化生成Fe3O4,失去8 NA个电子 | |
| C. | 常温常压下,14 g的CO和N2混合气体含有的原子数为NA | |
| D. | 常温常压下,22.4 L氧气与足量镁粉充分反应,转移的电子数为2NA |
分析 A、求出氯化钡的物质的量n=CV,然后根据1mol氯化钡中含2mol氯离子来分析;
B、铁反应生成四氧化三铁后变为+$\frac{8}{3}$价;
C、CO和氮气的摩尔质量均为28g/mol,且两者均为双原子分子;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答 解:A、溶液中氯化钡的物质的量n=CV=1mol/L×1L=1mol,而1mol氯化钡中含2mol氯离子,即2NA个,故A错误;
B、铁反应生成四氧化三铁后变为+$\frac{8}{3}$价,故1mol铁失去$\frac{8}{3}$mol电子即$\frac{8}{3}$NA个,故B错误;
C、CO和氮气的摩尔质量均为28g/mol,故14g混合物的物质的量为0.5mol,且两者均为双原子分子,故0.5mol混合物中含1mol原子即NA个,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L氧气的物质的量小于1mol,则和镁反应后转移的电子的物质的量小于4mol,个数小于4NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.下列化合物的俗称与化学式不对应的是( )
| A. | 纯碱-Na2CO3 | B. | 熟石灰-Ca(OH)2 | ||
| C. | 明矾-Al2(SO4)3•12H2O | D. | 胆矾-CuSO4•5H2O |
12.下列离子方程式的书写,正确的是( )
| A. | 金属铁与盐酸的反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氧化铜与硫酸溶液的反应:O2-+2H+═H2O | |
| C. | CuSO4溶液与Ba(OH)2溶液混合:Cu2++2OH-═Cu(OH)2↓ | |
| D. | 硫酸铝溶液与稀氨水混合:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
16.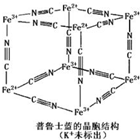 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )| A. | 化学式可以表示为KFe2(CN)6 | |
| B. | 每一个立方体中平均含有24个π键 | |
| C. | 普鲁士蓝不属于配位化合物 | |
| D. | 每个Fe3+周围与之相邻的Fe2+离子有12个 |
17.不用任何试剂就能鉴别的一组物质是( )
| A. | Na2CO3和NaHCO3 | B. | Na2CO3和NaCl | C. | Na2CO3和盐酸 | D. | NaHCO3和盐酸 |
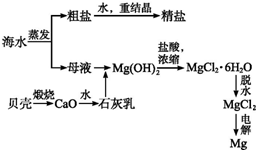 海水的综合利用可以制备金属镁,其流程如图所示:
海水的综合利用可以制备金属镁,其流程如图所示: