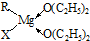题目内容
11.如图电解质溶液为稀硫酸,下列说法正确的是( )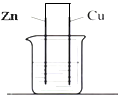
| A. | 该装置中Zn作为正极 | B. | 该装置可以实现电能转化为化学能 | ||
| C. | 电子从锌电极经过溶液到铜电极 | D. | 溶液中的H+移向铜电极 |
分析 铜锌原电池中,负极是活泼金属锌,正极是金属铜,电子从负极流向正极,氢离子移向正极得电子产生氢气,原电池装置将化学能转化为电能,据此分析.
解答 解:A.铜锌原电池中,负极是金属锌,正极是金属铜,故A错误;
B.原电池是将化学能转化为电能的装置,故B错误;
C.铜锌原电池中,负极是金属锌,正极是金属铜,电子从负极流向正极,即电子由锌电极经过导线到铜电极,故C错误;
D.由原电池的工作原理可知,阳离子移向原电池的正极,故D正确;
故选D.
点评 本题考查学生原电池的工作原理以及能量转化形式知识,可以根据教材知识来回答,注意电子不能通过电解质溶液.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
19.一块已被部分氧化为Na2O的钠块10.8g,将其投入一定量水中,最终得到含16g溶质的NaOH溶液,则原固体中氧化钠的质量是( )
| A. | 8.5 g | B. | 10.8 g | C. | 6.2 g | D. | 4.6 g |
16.下列四幅图的相关说法正确的是( )
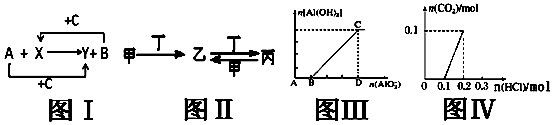

| A. | 关于图Ⅰ,已知C是氧气,X、Y是化合物,则A是钠,B是氢气 | |
| B. | 关于图Ⅱ,已知甲、乙、丙均含有相同的某种元素,若甲为NaOH溶液,则丁可能是CO2 | |
| C. | 关于图Ⅲ,表示NaAlO2溶液逐滴加入到NaOH溶液中,n(Al(OH)3)和n(AlO2-)之间的关系图象 | |
| D. | 关于图Ⅳ,表示各含0.1mol苏打和NaOH混合液中逐滴加入含溶质0.2mol的盐酸的关系图象 |
16.下列烃的命名中,正确的是( )
| A. | 2-乙基丁烷 | B. | 3,4-二甲基丁烷 | ||
| C. | 2,3,3-三甲基丁烷 | D. | 3-甲基-1-丁烯 |
17.下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
| 选项 | 微粒组 | 所加试剂 | 离子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O |
| B | Mg2+、Cl-、HCO3- | 过量NaOH溶液 | Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
| C | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+═SO2↑+H2O |
| D | K+、CO32-、NH3•H2O | 通入少量CO2 | CO32-+CO2+2H2O═2HCO3- |
| A. | A | B. | B | C. | C | D. | D |

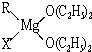 中的配位键
中的配位键