题目内容
标准状况下,一烧瓶中充满了HCl气体,做完喷泉实验后,发现水充满整个烧瓶。求所得溶液的物质的量浓度。若所得溶液的密度为1.02 g·cm-3,求溶液的溶质质量分数为多少。
解析:此题为一个无数据题,应抓住HCl气体的体积等于溶液的体积,气体的物质的量等于溶液中溶质的物质的量。
设气体的体积为1 L,则溶质的物质的量为![]() =
=![]() mol,
mol,
因为溶液的体积为1 L,所以溶质的物质的量浓度为:
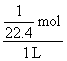 =
=![]() mol·L-1;
mol·L-1;
又因为溶质的质量为:![]() ×36.5 g·mol-1=
×36.5 g·mol-1=![]() g
g
溶液的质量为:
1.02 g·cm-3×1 L×1000 mL·L-1=1020 g
溶质的质量分数:![]() ×100%=0.16 %。
×100%=0.16 %。
求质量分数还有另一种方法——公式法。
物质的量浓度(mol·L-1)=![]()
溶质的质量分数= ×100%=0.16%
×100%=0.16%
若喷泉实验后,溶液未充满烧瓶,此时物质的量浓度、溶质的质量分数仍分别为![]() mol·L-1、0.16%。
mol·L-1、0.16%。
答案:![]() mol·L-1 0.16%
mol·L-1 0.16%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
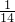 mol/L
mol/L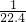 mol/L
mol/L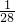 mol/L
mol/L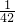 mol/L
mol/L