题目内容
(10分)
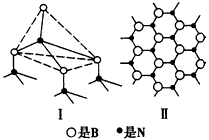
I. (6分)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
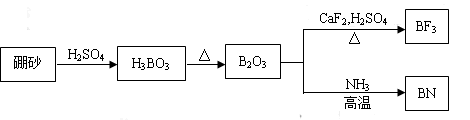
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是 、
;
(2) BN中B元素的化合价为 。
II. (4分)工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O
请根据题意填空:
(3)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填字母)。
A.气态氢化物的稳定性 B.最高价氧化物对应水化物的酸性
C.单质与氢气反应的难易 D.单质与同浓度酸发生反应的快慢
(4)2004年,美国科学家通过“勇气”号太空探测出火星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰与二氧化碳的结构相似,所有原子的最外层都满足8电子结构,且在氧气中会燃烧。请写出硫化羰的电子式 。
I. (6分)(1)
B2O3+3CaF2+3H2SO4 2BF3↑+3CaSO4+3H2O(2分)
2BF3↑+3CaSO4+3H2O(2分)
B2O3+2NH3 2BN+3
H2O(2分)
(2) +3(2分)
2BN+3
H2O(2分)
(2) +3(2分)
II. (4分)(1)
A C(2分)(2) (2分)
(2分)
【解析】I(1)考查了化学方程式的配平,注意条件、物质系数的书写
(2)由于N的非金属性较强,B显+3价,N显负价。
II(3)两种典型的非元素是O和F,一般是通过与氢气结合的难易及氢化物的稳定性来判断,由于两者均不具有最高价含氧酸,也就不能用最高价含氧酸的酸性强弱来比较了;
(4)对比CO2 很容易写出硫化羰的电子式:

 春雨教育同步作文系列答案
春雨教育同步作文系列答案(10分)
I.(6分)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是 、
;
(2) BN中B元素的化合价为 。
II. (4分)工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O
请根据题意填空:
(3)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填字母)。
| A.气态氢化物的稳定性 | B.最高价氧化物对应水化物的酸性 |
| C.单质与氢气反应的难易 | D.单质与同浓度酸发生反应的快慢 |
 ,则COCl2分子内含有_____个π键,C原子的杂化方式为____。
,则COCl2分子内含有_____个π键,C原子的杂化方式为____。