题目内容
5.下列各反应中,盐酸既表现出酸性又表现出还原性的是( )| A. | HCl+AgNO3═AgCl+HNO3 | B. | MnO2+4HCl(浓)═MnCl2+Cl2↑+H2O | ||
| C. | 2HCl$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | D. | Mg+2HCl═MgCl2+H2↑ |
分析 生成盐体现盐酸的酸性,生成氯气时Cl元素的化合价升高,体现HCl的还原性,以此来解答.
解答 解:A.只体现酸性,故A不选;
B.生成氯化锰体现酸性,生成氯气体现还原性,故B选;
C.H、Cl元素的化合价变化,体现氧化性、还原性,故C不选;
D.生成盐,且H元素的化合价降低,体现酸性和氧化性,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意HCl中元素的化合价变化,题目难度不大.

练习册系列答案
相关题目
16.物质的量浓度相同的下列溶液中,按pH由小到大顺序排列的是( )
| A. | Na2CO3、NaHCO3、NaCl、HCl | B. | Na2CO3、NaHCO3、HCl、NaCl | ||
| C. | (NH4)2SO4、NH4Cl、NaNO3、Na2CO3 | D. | NH4Cl、(NH4)2SO4、Na2CO3、NaNO3 |
13.下列说法正确的是( )
| A. | 19世纪初,化学家维勒提出了有机化学的概念 | |
| B. | 自然界存在或不存在的有机物都可以利用人工合成出来 | |
| C. | 有机化合物的定量分析法最早由瑞典化学家贝采里乌斯提出的 | |
| D. | 著名的有机合成化学家李比希曾说:“有机合成的威力体现为在老的自然界旁边再建立起一个新的自然界.” |
20.由乙醛和丁酸、乙酸乙酯三种有机物按一定比例组成的混合物中,若含氧的质量分数为A%,则此混合物中含碳的质量分数为( )
| A. | $\frac{6A%}{7}$ | B. | $\frac{(1-A%)}{7}$ | C. | $\frac{6(1-A%)}{7}$ | D. | (100-$\frac{7A}{6}$)% |
10.以下不能达到鉴别物质目的是( )
| A. | 用食醋鉴别食盐和纯碱 | |
| B. | 用丁达尔效应现象鉴别蛋白质溶液和蔗糖溶液 | |
| C. | 用Ca(OH)2溶液鉴别SO2、CO2气体 | |
| D. | 用硝酸银溶液鉴别溴蒸气和二氧化氮气体 |
15.氨是化肥工业和基本有机化工的主要原料,合成氨工业因此成为基本无机化工之一.回答下列问题:
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)
已知几个反应的能量变化如图所示,则上述反应的△H=c-5a-11bkJ•mol-1
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:
3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
现有甲、乙、丙3个固定容积为2L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
①下列描述不能说明该反应已达到平衡状态的是a.(填序号);
a.容器内混合气体的密度保持不变
b.3v正(N2)═v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=0.05mol•L-1•min-1,该温度下,反应的平衡常数K=5.33L2•mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是ac(填序号).
a.cl>c3 b.wl<w2 c.ρ2>ρ1>ρ3
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是将产物混合气中的氨冷却分离后,剩余气体循环使用.
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)
已知几个反应的能量变化如图所示,则上述反应的△H=c-5a-11bkJ•mol-1
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
现有甲、乙、丙3个固定容积为2L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol H2、2molN2 | 4mol H2、4molN2 | 2mol NH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| 平衡时N2的体积分数 | w1 | W2 | W3 |
| 混合气体的密度(g•L-1) | ρ1 | ρ2 | ρ3 |
a.容器内混合气体的密度保持不变
b.3v正(N2)═v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=0.05mol•L-1•min-1,该温度下,反应的平衡常数K=5.33L2•mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是ac(填序号).
a.cl>c3 b.wl<w2 c.ρ2>ρ1>ρ3
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是将产物混合气中的氨冷却分离后,剩余气体循环使用.
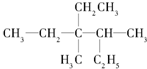 用系统命名法命名:3,4-二甲基-3-乙基己烷
用系统命名法命名:3,4-二甲基-3-乙基己烷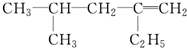
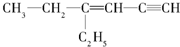 ,分子中饱和碳原子数为4,可能在同一平面上的碳原子数最多为8
,分子中饱和碳原子数为4,可能在同一平面上的碳原子数最多为8
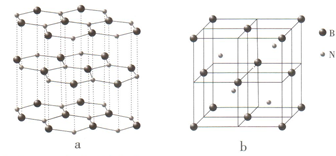 氮元素可形成丰富多彩的物质.
氮元素可形成丰富多彩的物质.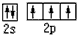 ;等物质的量的NH3和N2混合气体中σ键与π键的数目之比为2:1.
;等物质的量的NH3和N2混合气体中σ键与π键的数目之比为2:1.