题目内容
20.NA表示阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 1mol 苯乙烯中含有的碳碳双键数为4NA | |
| B. | 7.8g过氧化钠晶体中含有0.1NA个O22- | |
| C. | 标准状况下,22.4LNO2中含有NA个NO2分子 | |
| D. | 1 mol•L-1NH4Cl溶液中,NH4+<0的数目小于NA |
分析 A、苯乙烯中只有乙烯基中含双键;
B、求出过氧化钠的物质的量,然后根据过氧化钠中含2个钠离子和1个过氧根来分析;
C、NO2气体中存在平衡:2NO2?N2O4;
D、溶液体积不明确.
解答 解:A、苯乙烯中只有乙烯基中含一条双键,苯环中无碳碳双键,故1mol苯乙烯中含碳碳双键为NA条,故A错误;
B、7.8过氧化钠的物质的量为0.1mol,而过氧化钠中含2个钠离子和1个过氧根,故0.1mol过氧化钠中含0.1NA个过氧根,故B正确;
C、标况下22.4LNO2气体的物质的量为1mol,但NO2气体中存在平衡:2NO2?N2O4,故此1mol气体是NO2和N2O4的混合物,则其中含有NO2的分子个数小于NA个,故C错误;
D、溶液体积不明确,故溶液中的铵根离子的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.如表符号中“2”的含义正确的一组是( )
| 12H | 2Hc | Cl2 | Cu2+ | |
| A | 质量数 | 中子数 | 质子数 | 电荷数 |
| B | 质量数 | 质子数 | 原子数 | 电荷数 |
| C | 质子数 | 中子数 | 原子数 | 电子数 |
| D | 质量数 | 质子数 | 分子数 | 电荷数 |
| A. | A | B. | B | C. | C | D. | D |
8.分子式为C5H10O2的酯共有(不考虑立体异构)( )
| A. | 10种 | B. | 7种 | C. | 6种 | D. | 9种 |
12.下列说法不正确的是( )
| A. | 木炭在氧气中剧烈燃烧,生成黑色固体 | |
| B. | 铁丝在氧气中燃烧,火星四射 | |
| C. | 红磷在空气中燃烧,产生大量的白烟 | |
| D. | 硫在空气中燃烧,生成有刺激性气味气体 |
9.已知乙烯醇(CH2=CHOH)不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物,现有1mol乙二醇在一定条件下脱去1mol H2O,所得产物的结构简式有下列几种,其中不可能的是( )
①CH≡CH;②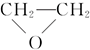 ③CH3CHO;④
③CH3CHO;④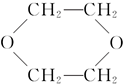 ⑤HO-CH2CH2OCH2CH2-OH.
⑤HO-CH2CH2OCH2CH2-OH.
①CH≡CH;②
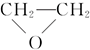 ③CH3CHO;④
③CH3CHO;④ ⑤HO-CH2CH2OCH2CH2-OH.
⑤HO-CH2CH2OCH2CH2-OH.| A. | 只有① | B. | 只有①④ | C. | 只有①⑤ | D. | ①②③④⑤ |
16.把V L含MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
| A. | $\frac{b-a}{V}$ mol•L-1 | B. | $\frac{2b-a}{V}$mol•L-1 | C. | $\frac{b-a}{V}$mol•L-1 | D. | $\frac{2(2b-a)}{V}$mol/L |
 .
.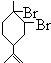 、
、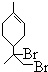 .(用键线式表示)
.(用键线式表示)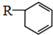 (R代表烃基),可能的结构共有4种.
(R代表烃基),可能的结构共有4种.