题目内容
NA为阿伏加德罗常数,下列说法正确的是(相对原子质量C-12 H-1)( )
| A、现有乙烯、丙烯的混合气体共28g,其原子总数为6NA |
| B、16g甲烷中含共用电子对的数目为4NA |
| C、1mol甲基的电子数目为10NA |
| D、标准状况下,11.2L四氯化碳所含的分子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.乙烯和丙烯的混合物的最简式为CH2,根据二者的最简式计算出混合气体中含有的原子总数;
B.甲烷分子中含有4个碳氢共用电子对,16个甲烷的物质的量为1mol,含有4mol共用电子对;
C.甲基的电子式为 ,甲基中含有9个电子,则1mol甲基中含有9mol电子;
,甲基中含有9个电子,则1mol甲基中含有9mol电子;
D.标准状况下四氯化碳为液体,不能使用标况下的气体摩尔体积计算四氯化碳的物质的量.
B.甲烷分子中含有4个碳氢共用电子对,16个甲烷的物质的量为1mol,含有4mol共用电子对;
C.甲基的电子式为
 ,甲基中含有9个电子,则1mol甲基中含有9mol电子;
,甲基中含有9个电子,则1mol甲基中含有9mol电子;D.标准状况下四氯化碳为液体,不能使用标况下的气体摩尔体积计算四氯化碳的物质的量.
解答:
解:A.28g乙烯和丙烯的混合物中含有2mol最简式CH2,含有2mol碳原子和4mol氢原子,总共含有6mol原子,原子总数为6NA,故A正确;
B.16g甲烷的物质的量为1mol,甲烷的电子式为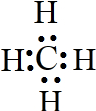 ,1mol甲烷中含有4mol碳氢共用电子对,含共用电子对的数目为4NA,故B正确;
,1mol甲烷中含有4mol碳氢共用电子对,含共用电子对的数目为4NA,故B正确;
C.1个甲基( )含有9个电子,1mol甲基(-CH3)所含的电子总数为9NA,故C错误;
)含有9个电子,1mol甲基(-CH3)所含的电子总数为9NA,故C错误;
D.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算11.2L四氯化碳的物质的量,故D错误;
故选AB.
B.16g甲烷的物质的量为1mol,甲烷的电子式为
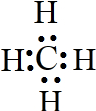 ,1mol甲烷中含有4mol碳氢共用电子对,含共用电子对的数目为4NA,故B正确;
,1mol甲烷中含有4mol碳氢共用电子对,含共用电子对的数目为4NA,故B正确;C.1个甲基(
 )含有9个电子,1mol甲基(-CH3)所含的电子总数为9NA,故C错误;
)含有9个电子,1mol甲基(-CH3)所含的电子总数为9NA,故C错误;D.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算11.2L四氯化碳的物质的量,故D错误;
故选AB.
点评:本题考查了阿伏伽德罗常数的判断及计算,题目难度中等,注意明确标况下气体摩尔体积的使用条件,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,选项C为易错点,注意羟基与氢氧根离子、甲基与甲烷、碳正离子之间的区别.

练习册系列答案
相关题目
某有机物的结构简式为 则该物质不能发生的反应有( )
则该物质不能发生的反应有( )
 则该物质不能发生的反应有( )
则该物质不能发生的反应有( )| A、加成反应 | B、消去反应 |
| C、水解反应 | D、氧化反应 |
下列有关说法中正确的是( )
| A、分子组成相差1个或者n个CH2原子团的有机物是同系物 |
| B、两种有机化合物的组成元素相同,各元素的质量分数也相同,二者一定是同分异构体 |
| C、分子式为C3H6Cl2和C3H2Cl6的同分异构体的数目相同 |
| D、甲苯能够被酸性高锰酸钾氧化,是因为甲基对苯环产生了影响 |
下列除去杂质的方法错误的是( )
①除去乙烷中少量的乙烯:催化剂条件下通入H2.
②乙醇中混有少量乙酸,加入氢氧化钠溶液后,分液
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
①除去乙烷中少量的乙烯:催化剂条件下通入H2.
②乙醇中混有少量乙酸,加入氢氧化钠溶液后,分液
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
| A、①②④ | B、①②③ |
| C、②③④ | D、①③④ |
把Ba(OH)2溶液滴入KAl(SO4)2溶液中,使SO42-恰好全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
| A、Al3+ |
| B、Al(OH)3 |
| C、[Al(OH)4]- |
| D、Al3+和Al(OH)3 |
常温下,下列说法不正确的是( )
| A、pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度 |
| B、0.1mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) |
| C、向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| D、常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c(Na+)=c(CH3COO-) |
乙醇和乙酸反应生成乙酸乙酯的反应中,乙醇分子中断裂的化学键是( )
| A、碳氢键 | B、碳碳键 |
| C、碳氧键 | D、氧氢键 |
下列各组物质中,不是同分异构体的是( )
| A、葡萄糖、果糖 |
| B、淀粉、纤维素 |
| C、硝基乙烷、氨基乙酸 |
| D、蔗糖、麦芽糖 |