题目内容
实验室中有两瓶溶液:一瓶是0.1mol?L-1的CH3COOH溶液,另一瓶是由0.2mol?L-1的CH3COONa溶液和0.2mol?L-1的盐酸等体积混合而成的溶液(混合时忽视溶液的体积变化).下列关于两溶液的c(H+)相对大小的叙述中,正确的是( )
| A、相等 | B、前者大于后者 |
| C、后者大于前者 | D、无法确定 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:在第一瓶溶液中,c1(CH3COOH)=0.1mol/L,
计算另一瓶混合溶液中醋酸浓度,比较二者大小,判断氢离子浓度大小.
计算另一瓶混合溶液中醋酸浓度,比较二者大小,判断氢离子浓度大小.
解答:
解:在第一瓶溶液中,c1(CH3COOH)=0.1mol/L,
在另一瓶溶液中:假设CH3COONa溶液和盐酸的体积均为VL,则:n(CH3COO-)=n(CH3COONa)=0.2mol.L-1×VL=0.2Vmol,
n(H+)=n(HCl)=0.2mol.L-1×VL=0.2Vmol,
由于CH3COO-+H+=CH3COOH
1mol 1mol 1mol
0.2Vmol 0.2Vmol 0.2Vmol
因此,CH3COONa溶液和盐酸混合后所得溶液中,
c2(CH3COOH)=0.2Vmol÷(V+V)L=0.1mol/L,
即c1(CH3COOH)=c2(CH3COOH)=0.1mol/L,故选A.
在另一瓶溶液中:假设CH3COONa溶液和盐酸的体积均为VL,则:n(CH3COO-)=n(CH3COONa)=0.2mol.L-1×VL=0.2Vmol,
n(H+)=n(HCl)=0.2mol.L-1×VL=0.2Vmol,
由于CH3COO-+H+=CH3COOH
1mol 1mol 1mol
0.2Vmol 0.2Vmol 0.2Vmol
因此,CH3COONa溶液和盐酸混合后所得溶液中,
c2(CH3COOH)=0.2Vmol÷(V+V)L=0.1mol/L,
即c1(CH3COOH)=c2(CH3COOH)=0.1mol/L,故选A.
点评:本题考查了物质的量浓度的计算,计算出混合后醋酸浓度是解题关键,较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关Fe2(SO4)3,溶液的叙述正确的是( )
| A、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| B、硫酸铁和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
| C、1L0.1mol/L该溶液和足量的Zn充分反应,生成11.2gFe |
| D、该溶液中,K+、Fe3+、C6H5OH、Br-可以大量共存 |
某无色透明溶液,能与Al作用放出H2,此溶液中可以大量共存的离子组是( )
| A、OH-、Mg2+、Ba2+、Cl- |
| B、SO42-、Na+、HCO3-、K+ |
| C、NO3-、OH-、Cl-、Ba2+ |
| D、Cu2+、H+、SO42-、NO3- |
如图图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确的是( )
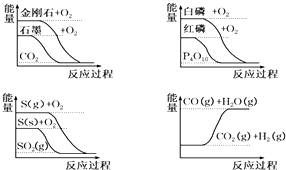

| A、金刚石比石墨稳定 |
| B、白磷转变为红磷是吸热反应 |
| C、相同物质的量的S(g)比S(s)完全反应时放热多 |
| D、CO(g)+H2O(g)═CO2(g)+H2(g) 该反应吸热 |
小明家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好.该佛像未被锈蚀的主要原因是( )
| A、铝不易发生化学反应 |
| B、铝的氧化物容易发生还原反应 |
| C、铝被氧化生成的氧化膜稳定且致密,保护着里面的铝 |
| D、铝的氧化物熔点很高 |
下列化学电池中,属于绿色电池的是( )
| A、锂电池 | B、锌锰电池 |
| C、镍镉电池 | D、碱性锌锰电池 |