题目内容
中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据计算PM2.5待测试样的pH= .
(2)NOx是汽车尾气的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图甲:

①N2(g)+O2(g)?2NO(g)△H= .
②当尾气中空气不足时,NOx在催化转化器中被还原成N2排出.写出NO被CO还原的化学方程式 .
③汽车汽油不完全燃烧时还产生CO,有人设想按下列反应除去CO:
2CO(g)═2C(s)+O2(g),已知该反应的△H>0,该设想能否实现? .
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图乙:
①用离子方程式表示反应器中发生的反应 .
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 .
③用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量、长寿命的镍氢电池.电池充放电时的总反应为:Ni(OH)2+M?放电充电 NiO(OH)+MH,电池放电时,负极电极反应式为 ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸.
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)NOx是汽车尾气的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图甲:

①N2(g)+O2(g)?2NO(g)△H=
②当尾气中空气不足时,NOx在催化转化器中被还原成N2排出.写出NO被CO还原的化学方程式
③汽车汽油不完全燃烧时还产生CO,有人设想按下列反应除去CO:
2CO(g)═2C(s)+O2(g),已知该反应的△H>0,该设想能否实现?
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图乙:
①用离子方程式表示反应器中发生的反应
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是
③用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量、长寿命的镍氢电池.电池充放电时的总反应为:Ni(OH)2+M?放电充电 NiO(OH)+MH,电池放电时,负极电极反应式为
考点:常见的生活环境的污染及治理,化学电源新型电池,pH的简单计算,氮的氧化物的性质及其对环境的影响
专题:化学反应中的能量变化,电化学专题,化学应用
分析:(1)根据溶液中电荷守恒计算H+离子浓度以及PH;
(2)①根据能量变化图计算反应热,反应热=吸收的能量-放出的能量;
②NO被CO还原,则CO被NO氧化生成二氧化碳和氮气,据此写出反应方程式;
③根据G=△H-T?△S判断反应能否自发进行;
(3)①由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HI;
②根据平衡移动的原理来分析;
③根据负极反应的特点和总电池反应来回答;
(2)①根据能量变化图计算反应热,反应热=吸收的能量-放出的能量;
②NO被CO还原,则CO被NO氧化生成二氧化碳和氮气,据此写出反应方程式;
③根据G=△H-T?△S判断反应能否自发进行;
(3)①由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HI;
②根据平衡移动的原理来分析;
③根据负极反应的特点和总电池反应来回答;
解答:
解:(1)溶液中电荷守恒:C(K+)+C(NH4+)+C(H+)=2C(SO42-)+C(NO3-)+C(Cl-),得C(H+)=1×10-4mol?L-1,pH值为4,
故答案为:4;
(2)①该反应中的反应热=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol;
故答案为:+183kJ?mol-1;
②在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:2CO+2NO
N2+2CO2;
故答案为:2CO+2NO
N2+2CO2;
③2CO(g)=2C(s)+O2(g),该反应是焓增、熵减的反应.根据G=△H-T?△S,G>0,不能实现,
故答案为:不能;
(3)①由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HI,离子方程式为:SO2+I2+2H2O═SO42-+2I-+4H+;
故答案为:SO2+I2+2H2O═SO42-+2I-+4H+;
②在膜分离器中发生反应:2HI?I2+H2,将H2分离出来有利于平衡向右移动,利于I2和H2的生成;
故答案为:有利于平衡向右移动,有利于碘和氢气的生成;
③负极反应物MH失去电子,生成的H+在碱性条件下生成H2O,电解反应式为:MH-e-+OH-=H2O+M;
故答案为:MH-e-+OH-=H2O+M.
故答案为:4;
(2)①该反应中的反应热=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol;
故答案为:+183kJ?mol-1;
②在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:2CO+2NO
| ||
故答案为:2CO+2NO
| ||
③2CO(g)=2C(s)+O2(g),该反应是焓增、熵减的反应.根据G=△H-T?△S,G>0,不能实现,
故答案为:不能;
(3)①由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HI,离子方程式为:SO2+I2+2H2O═SO42-+2I-+4H+;
故答案为:SO2+I2+2H2O═SO42-+2I-+4H+;
②在膜分离器中发生反应:2HI?I2+H2,将H2分离出来有利于平衡向右移动,利于I2和H2的生成;
故答案为:有利于平衡向右移动,有利于碘和氢气的生成;
③负极反应物MH失去电子,生成的H+在碱性条件下生成H2O,电解反应式为:MH-e-+OH-=H2O+M;
故答案为:MH-e-+OH-=H2O+M.
点评:本题较为综合,涉及化学反应方程式、离子方程式、热化学反应方程式、电极反应式的书写等知识点,注意反应热的计算方法,为易错点.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案
相关题目
最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),结合周期表知识,有关说法正确的是( )
A、羰基硫的电子式为 |
| B、羰基硫中含有非极性键 |
| C、羰基硫沸点比CO2低 |
| D、羰基硫中硫原子未满足8电子结构 |
下列物质属于有机物的是( )
| A、氰氨酸 |
| B、碳酸氢铵 |
| C、酒精 |
| D、KNO3 |
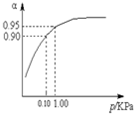 硫酸用途十分广泛,工业上合成硫酸时,将SO2转化为催化氧化是一个关键步骤.请回答下列问题:
硫酸用途十分广泛,工业上合成硫酸时,将SO2转化为催化氧化是一个关键步骤.请回答下列问题:
