题目内容
18.平衡常数的大小可以表示反应进行的程度,平衡常数越大,说明( )| A. | 反应物平衡浓度较大 | B. | 反应越有利于往逆反应方向进行 | ||
| C. | 反应进行的越彻底 | D. | 生成物平衡浓度较小 |
分析 平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,化学平衡常数只与温度有关,与浓度、压强无关,平衡常数越大,说明可逆反应进行的程度越大.
解答 解:化学平衡常数为产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,化学平衡常数表达式中,生成物浓度位于表达式的分子,反应物浓度位于表达式的分母,即化学平衡常数越大,则生成物平衡时浓度越大,反应物平衡时浓度越小,平衡常数越大,所以A、D错误,说明可逆反应正向进行的程度越大,则B错误,C正确,故选C.
点评 本题考查化学平衡常数表达式,化学平衡常数越大,则化学反应进行的程度越大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.能正确表示下列反应的离子方程式是( )
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H20+SO2═2NH4++SO32-+H2O | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+═2Fe3++3H2O |
10.组成和结构可用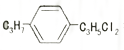 表示的有机物共有(不考虑立体结构)( )
表示的有机物共有(不考虑立体结构)( )
 表示的有机物共有(不考虑立体结构)( )
表示的有机物共有(不考虑立体结构)( )| A. | 16种 | B. | 18种 | C. | 20种 | D. | 22种 |
7. 环己烯是一种重要的化工原料.
环己烯是一种重要的化工原料.
(1)实验室可由环己醇制备环己烯,反应的化学方程式是 .
.
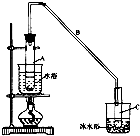
(2)实验装置如下图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.环己醇和环己烯的部分物理性质如下:
①A中碎瓷片的作用是防止暴沸;导管B除了导气外还具有的作用是冷凝.
②试管A置于水浴中的目的是受热均匀,便于控温;
试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.
 环己烯是一种重要的化工原料.
环己烯是一种重要的化工原料.(1)实验室可由环己醇制备环己烯,反应的化学方程式是
 .
.(2)实验装置如下图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.环己醇和环己烯的部分物理性质如下:
| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
②试管A置于水浴中的目的是受热均匀,便于控温;
试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.
8.取38.4g铜与适量的浓硝酸反应,铜全部反应后,共收集到22.4L(标准状况)气体,反应消耗HNO3的物质的量可能是( )
| A. | 1mol | B. | 1.6mol | C. | 2.2mol | D. | 2.4mol |
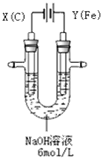 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示. 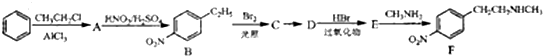
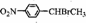 .
.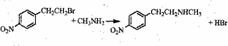 .
.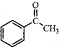 )常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线
)常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线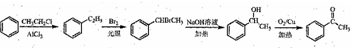 .
.