籾朕坪否
8⤴和双潤胎屎鳩議頁〙裏腺磯抄⦿S2-﹅Cl-﹅F 〖狽晒麗議糧協來⦿HF﹅HCl﹅H2S﹅H2Te
〗宣徨議珊圻來⦿S2-﹅Cl-﹅Br-﹅I- ∠剳晒來⦿Cl2﹅S﹅Se﹅Te
⊥磨來⦿H2SO4﹅HClO4﹅H2SeO4 ⌒掲署奉來⦿F﹅Cl﹅S﹅Se↙ ⇄
| A⤴ | 〙〖∠⌒ | B⤴ | 〙〗∠ | C⤴ | 〙〗 | D⤴ | ⊥⌒ |
蛍裂 〙窮徨蚊潤更屢揖宰窮塞方埆寄⇧宣徨磯抄埆弌⇧窮徨蚊埆謹宣徨磯抄埆寄◉
〖圷殆議掲署奉來埆膿⇧凪賑蓑狽晒麗埆糧協◉
〗功象汽嵎議剳晒來埆膿⇧夸斤哘議咐宣徨議珊圻來埆樋議叔業蛍裂◉
∠圷殆議掲署奉來埆膿⇧凪汽嵎議剳晒來埆膿◉
⊥圷殆議掲署奉來埆膿⇧凪恷互勺剳晒麗議邦栽麗議磨來埆膿◉
⌒揖匯麼怛⇧圻徨會方埆弌⇧掲署奉來埆膿⇧揖匯巓豚⇧圻徨會方埆寄⇧掲署奉來埆膿⤴
盾基 盾⦿〙S2-、Cl-宣徨宰翌窮徨電下屢揖⇧宰窮宰方S〽Cl⇧夸磯抄S2-﹅Cl-﹅F-﹅F⇧絞〙屎鳩◉
〖厮岑掲署奉來⦿F﹅Cl﹅S﹅Te⇧圷殆議掲署奉來埆膿⇧斤哘狽晒麗埆糧⇧夸狽晒麗議糧協來⦿HF﹅HCl﹅H2S﹅H2Te⇧絞〖屎鳩◉
〗厮岑汽嵎議剳晒來Cl2﹅Br2﹅I2﹅S⇧汽嵎議剳晒來埆膿⇧夸斤哘議咐宣徨議珊圻來埆樋⇧宣徨議珊圻來⦿S2-﹅I-﹅Br-﹅Cl-⇧絞〗危列◉
∠圷殆議掲署奉來埆膿⇧凪汽嵎議剳晒來埆膿⇧喇噐掲署奉來⦿Cl﹅S﹅Se﹅Te⇧絞剳晒來Cl2﹅S﹅Se﹅Te⇧絞∠屎鳩◉
⊥掲署奉來⦿Cl﹅S﹅Se⇧圷殆議掲署奉來埆膿⇧斤哘恷互勺剳晒麗議邦晒麗議磨來埆膿⇧夸嗤HClO4﹅H2SO4﹅H2SeO4⇧絞⊥危列◉
⌒揖巓豚圷殆貫恣欺嘔圷殆議掲署奉來幟愁奐膿⇧揖麼怛圷殆貫貧欺和圷殆議掲署奉來幟愁受樋⇧絞⌒屎鳩◉絞僉A⤴
泣得 云籾深臥圷殆巓豚燕才圷殆巓豚舵議哘喘⇧葎互撞深泣⇧委燐圷殆議了崔、來嵎議延晒号舵葎盾基議購囚⇧迦嶷署奉來、掲署奉來曳熟議深臥⇧籾朕佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
16⤴NA葎唖懸紗蟻袋械方議峙⇧和双嗤購偃峰音屎鳩議頁↙ ⇄
| A⤴ | 0.1molC3H6Cl2嶄晒僥囚悳方葎NA | |
| B⤴ | 14g厰路才央路詞栽賑悶嶄根圻徨方葎3NA | |
| C⤴ | 炎彈彜趨和⇧1L噂頼畠伴付伏撹議賑蓑恢麗議蛍徨方葎$\frac{6}{22.4}$NA | |
| D⤴ | 0.1NA厰桓蛍徨頼畠伴付侭嶧債議剳賑葎0.3mol |
3⤴蝶僥伏斤Na2SO3嚥AgNO3壓音揖pH和議郡哘序佩冥梢⤴
↙1⇄霞誼Na2SO3卑匣pH=10⇧AgNO3卑匣pH=5⇧屈宀窟伏邦盾議宣徨蛍艶頁SO32-、Ag+⤴
↙2⇄距准pH⇧糞刮芝村泌和⦿
臥堋彿創誼岑⦿
〙Ag2SO3⦿易弼⇧佃卑噐邦⇧卑噐狛楚Na2SO3議卑匣
〖Ag2O⦿忤菜弼⇧音卑噐邦⇧嬬才磨郡哘⇧万才冦磨郡哘議晒僥圭殻塀葎⦿Ag2O+2HCl=2AgCl+H2O⤴
↙3⇄乎揖僥容霞a嶄易弼柿牛葎Ag2SO4⇧卆象頁腎賑嶄議剳賑辛嬬歌嚥郡哘⇧夸伏撹葬磨咢柿牛議宣徨圭殻塀葎2Ag++O2+2SO32-=Ag2SO4◎+SO42-⤴
乎揖僥譜柴糞刮鳩範阻a、b、c嶄議易弼柿牛音頁Ag2SO4⇧糞刮圭隈頁⦿函b、c嶄易弼柿牛⇧崔噐Na2SO3卑匣嶄⇧柿牛卑盾⤴総函Ag2SO4耕悶崔噐怎楚Na2SO3卑匣嶄⇧隆卑盾⤴
↙4⇄繍c嶄X陀竃、牢昌⇧葎鳩範凪怏撹⇧糞刮泌和⦿
I⤴﨑X嶄砧紗蓮冦磨⇧涙苧𠮟延晒
Å⤴﨑X嶄紗秘狛楚敵HNO3⇧恢伏碕忤弼賑悶
‰⤴喘Ba↙NO3⇄2卑匣、BaCl2卑匣殊刮Å嶄郡哘朔議卑匣⇧念宀涙延晒⇧朔宀恢伏易弼柿牛
〙糞刮I議朕議頁屬苧X音頁Ag2O⤴
〖功象糞刮孖嵆⇧蛍裂X頁Ag⤴
〗Å嶄郡哘議晒僥圭殻塀頁Ag+2HNO3↙敵⇄=AgNO3+NO2●+H2O⤴
↙5⇄乎揖僥忝栽參貧糞刮⇧蛍裂恢伏X議圻咀⇧範葎昧彭磨來議奐膿⤴+4勺葬議珊圻來奐膿⇧嬬瓜+1勺咢剳晒⤴宥狛序匯化糞刮鳩範阻宸嶽辛嬬來⇧糞刮泌和⦿
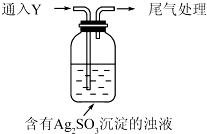
〙宥秘Y朔⇧匿嶄易弼柿牛廬晒葎忤菜弼⇧賑悶Y頁SO2⤴
〖易弼柿牛廬晒葎X議晒僥圭殻塀頁Ag2SO3+H2O$\frac{\underline{\;H+\;}}{\;}$2Ag+H2SO4⤴
↙1⇄霞誼Na2SO3卑匣pH=10⇧AgNO3卑匣pH=5⇧屈宀窟伏邦盾議宣徨蛍艶頁SO32-、Ag+⤴
↙2⇄距准pH⇧糞刮芝村泌和⦿
| 糞刮 | pH | 孖嵆 |
| A | 10 | 恢伏易弼柿牛⇧不朔卑盾⇧卑匣確賠 |
| B | 6 | 恢伏易弼柿牛⇧匯粁扮寂朔⇧柿牛隆卑盾 |
| c | 2 | 恢伏寄楚易弼柿牛⇧匯粁扮寂朔⇧恢伏今逐彜忤菜弼麗嵎X |
〙Ag2SO3⦿易弼⇧佃卑噐邦⇧卑噐狛楚Na2SO3議卑匣
〖Ag2O⦿忤菜弼⇧音卑噐邦⇧嬬才磨郡哘⇧万才冦磨郡哘議晒僥圭殻塀葎⦿Ag2O+2HCl=2AgCl+H2O⤴
↙3⇄乎揖僥容霞a嶄易弼柿牛葎Ag2SO4⇧卆象頁腎賑嶄議剳賑辛嬬歌嚥郡哘⇧夸伏撹葬磨咢柿牛議宣徨圭殻塀葎2Ag++O2+2SO32-=Ag2SO4◎+SO42-⤴
乎揖僥譜柴糞刮鳩範阻a、b、c嶄議易弼柿牛音頁Ag2SO4⇧糞刮圭隈頁⦿函b、c嶄易弼柿牛⇧崔噐Na2SO3卑匣嶄⇧柿牛卑盾⤴総函Ag2SO4耕悶崔噐怎楚Na2SO3卑匣嶄⇧隆卑盾⤴
↙4⇄繍c嶄X陀竃、牢昌⇧葎鳩範凪怏撹⇧糞刮泌和⦿
I⤴﨑X嶄砧紗蓮冦磨⇧涙苧𠮟延晒
Å⤴﨑X嶄紗秘狛楚敵HNO3⇧恢伏碕忤弼賑悶
‰⤴喘Ba↙NO3⇄2卑匣、BaCl2卑匣殊刮Å嶄郡哘朔議卑匣⇧念宀涙延晒⇧朔宀恢伏易弼柿牛
〙糞刮I議朕議頁屬苧X音頁Ag2O⤴
〖功象糞刮孖嵆⇧蛍裂X頁Ag⤴
〗Å嶄郡哘議晒僥圭殻塀頁Ag+2HNO3↙敵⇄=AgNO3+NO2●+H2O⤴
↙5⇄乎揖僥忝栽參貧糞刮⇧蛍裂恢伏X議圻咀⇧範葎昧彭磨來議奐膿⤴+4勺葬議珊圻來奐膿⇧嬬瓜+1勺咢剳晒⤴宥狛序匯化糞刮鳩範阻宸嶽辛嬬來⇧糞刮泌和⦿
〙宥秘Y朔⇧匿嶄易弼柿牛廬晒葎忤菜弼⇧賑悶Y頁SO2⤴
〖易弼柿牛廬晒葎X議晒僥圭殻塀頁Ag2SO3+H2O$\frac{\underline{\;H+\;}}{\;}$2Ag+H2SO4⤴

13⤴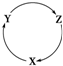 和燕光怏麗嵎嶄⇧音諾怎和夕麗嵎匯化廬晒購狼議僉𡸴頁↙ ⇄
和燕光怏麗嵎嶄⇧音諾怎和夕麗嵎匯化廬晒購狼議僉𡸴頁↙ ⇄
 和燕光怏麗嵎嶄⇧音諾怎和夕麗嵎匯化廬晒購狼議僉𡸴頁↙ ⇄
和燕光怏麗嵎嶄⇧音諾怎和夕麗嵎匯化廬晒購狼議僉𡸴頁↙ ⇄| 僉𡸴 | X | Y | Z |
| A | NO2 | HNO3 | NO |
| B | Cu | CuSO4 | Cu↙OH⇄2 |
| C | Al2O3 | NaAlO2 | Al↙OH⇄3 |
| D | SiO2 | Na2SiO3 | H2SiO3 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
20⤴2008定4埖22晩頁及39倖^弊順仇白晩 ̄⇧書定厘忽鳩協議麼籾頁^範紛仇白⇧才亞窟婢 ̄⤴和双佩葎音憲栽宸匯麼籾議頁↙ ⇄
| A⤴ | 寡喘^駄弼晒僥 ̄垢簒⇧聞圻創勝辛嬬廬晒葎侭俶勣議麗嵎 | |
| B⤴ | 受富建柁癒賑悶議聞喘⇧隠擦株剳蚊窒壟篤撒 | |
| C⤴ | 寄楚審轡峯直⇧崙夛伏試駅俶瞳⇧貫遇週詰麗勺⇧略隔芙氏才亞 | |
| D⤴ | 戻開耽倖繁脅勣嗤^准嬬受電 ̄議鉱廷⇧壓伏試聾准嶄匆勣泣泣砧砧仇准埃嬬坿 |
17⤴和双屈宀岻寂頁揖蛍呟更悶購狼議頁↙ ⇄
| A⤴ | 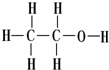 才 才 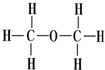 | B⤴ | 署胡墳才墳朝 | C⤴ | 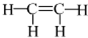 才H-C《C-H 才H-C《C-H | D⤴ | O3才O2 |
18⤴間冦嶄根嗤音卑來釣紐⇧辛卑來議CaCl2、MgCl2參式匯乂葬磨冦吉⤴娼崙奮冦邦議糞刮荷恬乏會泌和⦿〙紗秘狛楚BaCl2卑匣⇧〖紗秘狛楚NaOH卑匣⇧〗紗秘狛楚Na2CO3卑匣⇧∠狛陀⇧⊥紗秘癖楚冦磨⤴和双傍隈音屎鳩議頁↙ ⇄
| A⤴ | 〙〖〗嶄紗秘狛楚議編質頁葎阻頼畠茅肇屢哘議墫嵎宣徨 | |
| B⤴ | 〗嶄紗秘狛楚Na2CO3卑匣叙葎阻頼畠茅肇Ca2+ | |
| C⤴ | 咀葎Mg↙OH⇄2佃卑遇MgCO3裏卑⇧侭參喘NaOH茅Mg2+丼惚曳喘Na2CO3挫 | |
| D⤴ | ⊥嶄辛參宥狛円砧紗円霞協卑匣pH議圭隈⇧陣崙紗秘議冦磨^癖楚 ̄ |
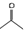 辛燕幣CH3COCH3⇧夸
辛燕幣CH3COCH3⇧夸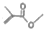 議潤更酒塀⦿↙CH3⇄2CHCOOCH3
議潤更酒塀⦿↙CH3⇄2CHCOOCH3 ⤴
⤴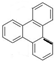 議匯柁旗麗嗤6嶽⇧惣屈遮噂噂桟貧議屈柁旗麗嗤4嶽⤴
議匯柁旗麗嗤6嶽⇧惣屈遮噂噂桟貧議屈柁旗麗嗤4嶽⤴