题目内容
下列反应属于加成反应的是( )
A、CH2=CH2+HBr
| |||
B、 +Br2 +Br2
 +HBr +HBr | |||
C、2CH3CH2OH+O2
| |||
D、CH4+2Cl2
|
考点:取代反应与加成反应
专题:有机反应
分析:有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,根据定义分析解答.
解答:
解:A、乙烯与溴化氢发生了加成反应,化学键由不饱和的碳碳双键变成了碳碳单键,故A正确;
B、苯与溴发生了取代反应生成溴苯,不属于加成反应,故B错误;
C、乙醇与氧气反应生成乙醛,属于氧化反应,故C错误;
D、甲烷与氯气发生取代反应,故D错误;
故选A.
B、苯与溴发生了取代反应生成溴苯,不属于加成反应,故B错误;
C、乙醇与氧气反应生成乙醛,属于氧化反应,故C错误;
D、甲烷与氯气发生取代反应,故D错误;
故选A.
点评:本题主要考查了常见有机反应类型的判断,题目难度不大,注意明确常见有机反应的类型及判断方法,明确含双键、苯环的物质能发生加成反应.

练习册系列答案
相关题目
下列物质中含有原子数由多到少排列正确的是( )
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
| A、①②③④ | B、④③②① |
| C、②③④① | D、②④③① |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,2.24 L 水中所含的电子数为NA |
| B、常温常压下,16 g O3所含的电子数为8NA |
| C、0.1 mol Na2O2 晶体中所含的离子数为0.4NA |
| D、1 mol Fe在氧气中充分燃烧失去的电子数为3NA |
下列物质分类的正确组合是( )
| 碱 | 酸 | 盐 | 酸性氧化物 | 碱性氧化物 | |
| A. | Na2CO3 | H2SO4 | NaOH | CO2 | SO2 |
| B. | NaOH | HCl | NaCl | CO | Na2O |
| C | NaOH | CH3COOH | CaF2 | SO2 | CO |
| D. | KOH | HNO3 | CaCO3 | SO3 | CaO |
| A、A | B、B | C、C | D、D |
在下列条件下,两瓶气体所含的原子数一定相等的是( )
| A、具有同压强、同体积的N2O和CO2 |
| B、具有同温度、同体积的CO和N2 |
| C、具有同体积、同密度的SO2和NO2 |
| D、具有同质量、不同密度的O2和O3 |
已知:P4(s、白磷)+5O2(g)═P4O10(s)△H=-2983.2kJ/mol;4P(s、红磷)+5O2(g)═P4O10(s)△H=-2954kJ/mol;那么,1mol白磷转变成相应物质的量红磷时,应是( )
| A、吸收29.2kJ热量 |
| B、放出29.2kJ热量 |
| C、放出7.3kJ热量D.吸收7.3kJ热量 |
| D、101 kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,反应达到平衡后,改变某一个条件,如图示意图曲线①~⑧中正确的是( )
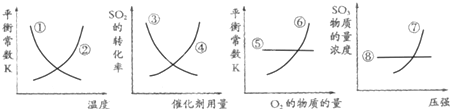

| A、①⑥⑧ | B、①⑤⑦ |
| C、②③④ | D、③⑥⑦ |
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
下列叙述错误的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A、容器①、②中反应的平衡常数相等 |
| B、平衡时,两个容器中NH3的体积分数相等 |
| C、容器②中达平衡时放出的热量Q=23.15 kJ |
| D、若容器①体积为0.5 L,则平衡时放出的热量<23.15 kJ |
下列各项表达式正确的是( )
A、O2-的结构示意图: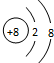 |
B、Na2S的电子式: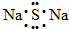 |
| C、甲醛的结构简式:CH2O |
D、氮分子的结构式: |