题目内容
8.MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液,阴极的电极反应式是2H++2e-=H2↑.若电解电路中通过2mol电子,MnO2的理论产量为87g.分析 用石墨作电极电解酸化的MnSO4溶液,阴极上首先放电的是H+,生成H2;阳极上Mn 2+失电子和水反应生成MnO2和H+;
根据MnO2和转移电子之间关系式计算MnO2理论产量.
解答 解:阴极上得电子,发生还原反应,H+得电子生成氢气,电极反应式为2H++2e-=H2↑,阳极上Mn 2+失电子和水反应生成MnO2和H+,则阳极反应式为:MnSO4-2e-+2H2O═MnO2+SO42-+4H+,
因为MnSO4~MnO2~2e-,通过2mol电子产生1molMnO2,其质量=1mol×87g/mol,
故答案为:2H++2e-=H2↑;87.
点评 本题考查电解原理,为高频考点,侧重考查分析和计算,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,知道各个物理量之间关系,题目难度不大.

练习册系列答案
相关题目
19.下列物质属于纯净物的是( )
| A. | 福尔马林 | B. | 甘油 | C. | 煤 | D. | 天然气 |
16.化学是一门与社会、生活、科研密切相关的自然科学.下列有关叙述中,不正确的是( )
| A. | 大量使用燃煤发电是形成雾霾的主要原因之一 | |
| B. | 天然气、煤气大量泄漏遇到明火会爆炸 | |
| C. | 利用化学反应可实现12C到14C的转化 | |
| D. | 因为氨易液化,在汽化时会吸收大量的热量,所以可作制冷剂 |
3.可逆反应:3A?3B+C△H>0,已知反应物A为气态物质,随着温度的升高,反应体系中气体的平均相对分子质量有变小趋势,则下列判断中,正确的是( )
①若C为固体,则B一定是气体 ②B和C一定都是气体
③B和C可能都是固体 ④B和C可能都是气体.
①若C为固体,则B一定是气体 ②B和C一定都是气体
③B和C可能都是固体 ④B和C可能都是气体.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
13.实验室欲用Na2CO3•10H20晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )
| A. | 要完成实验需称取10.6gNa2CO3•10H20晶体 | |
| B. | 本实验需用到的仪器只有药匙、玻璃棒、烧杯、胶头滴管和100 mL容量瓶 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时用胶头滴管滴人的蒸馏水滴在容量瓶内部刻度线上方会导致浓度偏低 |
20.获得“863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,相关论文发表在J.Am.Chem.Soc.(128,8720~8721,2006)上,已知电池总反应式为2Al+3I2═2AlI3.下列说法不正确的是( )
| A. | 该电池负极的电极反应为:Al-3e-═Al3+ | |
| B. | 该电池可能是一种可充电的二次电池 | |
| C. | 消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 | |
| D. | 电池工作时,溶液中铝离子向正极移动 |
17.在含2molH2SO4的浓硫酸中加入足量的锌粉,使其充分反应,下列推断中错误的是( )
①放出的气体除SO2外还有H2 ②只放出1molSO2气体 ③反应结束时转移4mol电子.
①放出的气体除SO2外还有H2 ②只放出1molSO2气体 ③反应结束时转移4mol电子.
| A. | ① | B. | ② | C. | ②③ | D. | ①② |
2.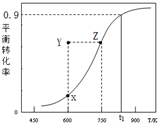 甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示.下列有关说法正确的是( )
甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示.下列有关说法正确的是( )
 甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示.下列有关说法正确的是( )
甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示.下列有关说法正确的是( )| A. | 脱氢反应的△H<0 | B. | 在t1K时,该反应的平衡常数为8.1 | ||
| C. | 600K时,Y点甲醇的υ(正)<υ(逆) | D. | 若增大体系压强,曲线将向上平移 |
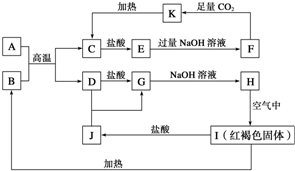 已知A~K均为中学化学的常见物质,它们之间的转化关系如下图所示,其中A是铝,且A+B→C+D是置换反应,反应过程中生成的水及其他部分产物已略去.
已知A~K均为中学化学的常见物质,它们之间的转化关系如下图所示,其中A是铝,且A+B→C+D是置换反应,反应过程中生成的水及其他部分产物已略去.