题目内容
19.室温下,下列事实不能说明NH3•H2O为弱电解质的是( )| A. | 0.1 mol•L-1 NH3•H2O的pH小于13 | |
| B. | 0.1 mol•L-1 NH4Cl的pH小于7 | |
| C. | 相同条件下,浓度均为0.1 mol•L-1 NaOH溶液和氨水,氨水的导电能力弱 | |
| D. | 0.1 mol•L-1 NH3•H2O能使无色酚酞试液变红色 |
分析 部分电离的电解质为弱电解质,只要能证明NH3.H2O部分电离就说明NH3.H2O是弱电解质,据此分析解答.
解答 解:A.0.1 mol•L-1 NH3•H2O的pH小于13,则溶液中c(OH-)<0.1mol/L,所以c(OH-)<c(NH3.H2O),说明NH3•H2O部分电离,为弱电解质,故A不选;
B.0.1 mol•L-1 NH4Cl的pH小于7显酸性,说明 NH4Cl是强酸弱碱盐,则证明NH3•H2O是弱电解质,故B不选;
C.相同条件下,浓度均为0.1 mol•L-1 NaOH溶液和氨水,氨水的导电能力弱,说明NH3•H2O部分电离,为弱电解质,故C不选;
D.0.1 mol•L-1 NH3•H2O能使无色酚酞试液变红色,说明NH3•H2O显碱性,则不能证明NH3.H2O是弱电解质,故D选;
故选D.
点评 本题考查了强弱电解质的判断,根据电解质的电离程度划分强弱电解质,不能根据电解质溶液的导电性强弱及物质的溶解性强弱判断强弱电解质,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列有机物的命名正确的是( )
| A. | 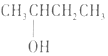 2--羟基丁烷 2--羟基丁烷 | B. | 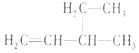 3--乙基--1--丁烯 3--乙基--1--丁烯 | ||
| C. | 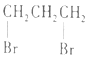 1,3--二溴丙烷 1,3--二溴丙烷 | D. | 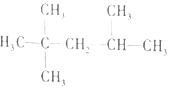 2,2,3--三甲基戊烷 2,2,3--三甲基戊烷 |
7.下列属于盐的是( )
| A. | NaCl | B. | KOH | C. | HNO3 | D. | CO2 |
14.已知:X(g)+2Y(g)?3Z(g)△H=-a KJ•mol-1(a>0).下列说法不正确的是( )
| A. | 0.1 mol X和0.2 mol Y充分反应生成Z的物质的量一定小于0.3 mol | |
| B. | 达到化学平衡状态时,X、Y、Z的浓度不再发生变化 | |
| C. | 达到化学平衡状态时,反应放出的总热量可达a kJ | |
| D. | 升高反应温度,逆反应速率增大,正反应速率减小 |
4.下列有关溶液中粒子浓度关系的叙述正确的是( )
| A. | 0.1mol•L-1NH4NO3溶液中:c(NH4+)>c(NO3-)>c(H+)>c(OH-) | |
| B. | 溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(CO32-)+c(HCO3-)+c( H2CO3) | |
| C. | 向10mL0.2mol•L-1NaCl溶液中滴入2mL0.1mol•L-1AgNO3溶液,溶液中离子浓度大小关系:c(Na+)>c(NO3-)=c(Cl-)>c(Ag+) | |
| D. | 常温下pH=2的醋酸与pH=12的烧碱溶液等体积混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
1.酒中含有酒精,酒精是一种危险物品,属于( )
| A. |  | B. |  | C. |  | D. |  |
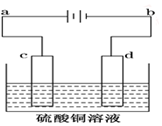 电解装置如图所示:
电解装置如图所示:
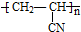 )混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.
)混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.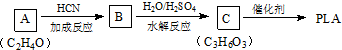
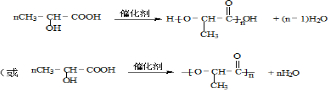 .
.