题目内容
18.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| B. | 2L 0.5mol/L亚硫酸溶液中含有的H+两种数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
分析 A、二氧化锰只能与浓盐酸反应,与稀盐酸不反应;
B、亚硫酸是弱电解质,不能完全电离;
C、过氧化钠与水反应生成氧气时,氧元素的价态由-1价变为0价;
D、NO和氧气反应生成NO2后,NO2存在平衡:2NO2?N2O4;
解答 解:A、二氧化锰只能与浓盐酸反应,与稀盐酸不反应,故盐酸不能完全反应,则转移的电子数小于0.3NA个,故A错误;
B、亚硫酸是弱电解质,不能完全电离,故溶液中的氢离子的个数小于2NA个,故B错误;
C、过氧化钠与水反应生成氧气时,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时转移0.2mol电子即0.2NA个,故C正确;
D、2molNO与1molO2充分反应生成2molNO2后,NO2存在平衡:2NO2?N2O4,导致分子个数小于2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列关于电解质分类的组合中,完全正确的是( )
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | HClO | HNO3 |
| 弱电解质 | HF | BaSO4 | CaCO3 | CH3COOH |
| 非电解质 | Cl2 | CS2 | C2H5OH | SO2 |
| A. | A | B. | B | C. | C | D. | D |
6.下列说法正确的是( )
| A. | 熔点:Na-K合金<Na<氯化钠 | |
| B. | 非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 | |
| D. | 同一原子中,2p、3p、4p能级的轨道数依次增多 |
13.下列实验的装置或操作正确的是( )
| A. |  分解NaHCO3 | B. |  转移溶液 | ||
| C. |  分离水和四氯化碳 | D. |  干燥CO2 |
9.下列反应中属于氧化还原反应,而且水既不作氧化剂又不作还原剂的是( )
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | SO3+H2O═H2SO4 | D. | 2Na+2H2O═2NaOH+H2↑ |
5.下列有关电池的说法,不正确的是( )
| A. | 智能手机上用的锂离子电池属于二次电池 | |
| B. | 碱性锌锰干电池中,锌电极是负极 | |
| C. | 铅蓄电池中,Pb02做负极 | |
| D. | 铜锌原电池(稀硫酸做电解质)工作时,锌电极发生氧化反应 |
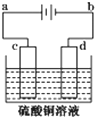 (1)电镀时,镀件与电源的负极连接.
(1)电镀时,镀件与电源的负极连接.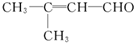 含氧官能团有醛基.
含氧官能团有醛基.