题目内容
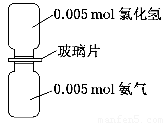
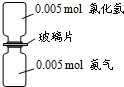
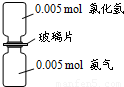
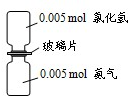 如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )| A、气体反应物的总体积为0.224L | B、产物中所含的N-H键个数为0.015NA | C、生成物的物质的量为0.005mol | D、加水溶解后所得溶液中NH4+浓度为0.005mol?L-1 |
分析:抽走玻璃片充分反应,恰好生成0.005molNH4Cl固体,没有气体剩余,结合物质中存在4个N-H及c=
解答.
| n |
| V |
解答:解:抽走玻璃片充分反应,恰好生成0.005molNH4Cl固体,
A.没有气体剩余,故A错误;
B.产物中所含的N-H键个数为0.005mol×4×NA=0.02NA,故B错误;
C.由NH3+HCl=NH4Cl可知,生成物的物质的量为0.005mol,故C正确;
D.溶液的体积未知,不能计算溶液中NH4+浓度,故D错误;
故选C.
A.没有气体剩余,故A错误;
B.产物中所含的N-H键个数为0.005mol×4×NA=0.02NA,故B错误;
C.由NH3+HCl=NH4Cl可知,生成物的物质的量为0.005mol,故C正确;
D.溶液的体积未知,不能计算溶液中NH4+浓度,故D错误;
故选C.
点评:本题考查物质的量有关计算,为高频考点,把握反应生成氯化铵固体及其物质的量为解答的关键,侧重分析能力及计算能力的考查,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
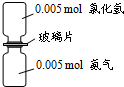 (2012?浦东新区二模)如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
(2012?浦东新区二模)如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )