题目内容
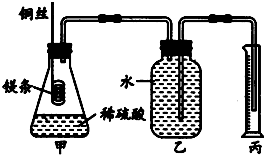 化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).
化学兴趣小组设计测定镁原子的摩尔质量的实验,简易装置如图,除去表面氧化膜的镁条质量为0.24g,镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积).(1)如何检查该装置的气密性?
(2)根据实验数据可得出镁的摩尔质量为
考点:实验装置综合,摩尔质量
专题:实验设计题
分析:(1)如果装置的气密性良好,则锥形瓶在受热时会后气体膨胀进入广口瓶,据此分析.
(2)设出镁的摩尔质量,根据化学方程式中的计量关系求算.
(2)设出镁的摩尔质量,根据化学方程式中的计量关系求算.
解答:
解:(1)如果装置的气密性良好,则锥形瓶在受热时会后气体膨胀进入广口瓶,则广口瓶中的短导管会有气泡,待放手后,锥形瓶内的气体冷缩,则压强变小,短导管中的水柱应高出液面,故答案为:两手掌紧贴锥形瓶外壁一会儿,如观察到广口瓶中短导管中有气泡产生,放手后有一段水柱高出液面,表明装置不漏气.
(2)设镁的摩尔质量为Xg/mol,根据镁与酸的反应:
Mg+2H+=Mg2++H2↑
1 1
mol 0.01mol
可有:
=
解得X=24g/mol
故答案为:24.
(2)设镁的摩尔质量为Xg/mol,根据镁与酸的反应:
Mg+2H+=Mg2++H2↑
1 1
| 0.24 |
| X |
可有:
| 1 | ||
|
| 1 |
| 0.01 |
解得X=24g/mol
故答案为:24.
点评:本题考查了装置气密性的检验和摩尔质量的有关求算,根据化学方程式的计量数的关系求算是常考点,难度不大.

练习册系列答案
相关题目
下列产品的使用不会对环境造成污染的是( )
| A、含磷洗衣粉 | B、酒精 |
| C、氟利昂 | D、含汞电池 |
用石墨做电极电解饱和食盐水,阳极电极反应式为( )
| A、Na++e--=Na |
| B、2H++4e-=2H2 |
| C、2Cl--2e-=Cl2 |
| D、4OH--4e-=2H2O+O2 |
酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+ Cl2→2Cl-HNO3→NO.MnO4-→
Mn2+ 分别用等物质的量的这些物质氧化足量的KI,得到I2最多 的是( )
Mn2+ 分别用等物质的量的这些物质氧化足量的KI,得到I2最多 的是( )
| A、Fe3+ |
| B、HNO3 |
| C、Cl2 |
| D、MnO4- |
0.5L 1mol/L的FeCl3溶液与0.2L 1mol/L的KCl溶液中,Cl-浓度比为( )
| A、15:2 | B、1:2 |
| C、3:1 | D、1:3 |
下列过程表达式中,属于电离方程式的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、HS-+H2O?S2-+H3O+ |
| C、NH3+H+=NH4+ |
| D、HSO3-+OH-=H2O+SO32- |
下列离子方程式书写不正确的是( )
| A、碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O | ||||
| B、含等物质的量的硫酸氢钠与氢氧化钡两溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | ||||
| C、用稀硝酸浸泡做过银镜反应的试管:3Ag+4H++NO3-=3Ag++NO↑+2H2O | ||||
D、用两个铜电极电解饱和食盐水:2Cl-+2H2O
|