题目内容
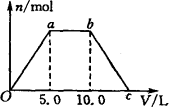
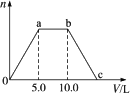
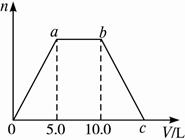
向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成的沉淀的物质的量(n)和通入CO2气体体积(V)的关系如下图,试完成下列问题: 
(1)a点之前的反应的离子方程式为:___________________________________________。
(2)a点到b点之间的离子反应方程式是:________________________________________。
(3)c点的二氧化碳体积是_______________L。
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为_______________。
思路解析:根据a之前反应的离子方程式是:Ba2++CO2+2OH-![]() BaCO3↓+H2O,可知n〔Ba(OH)2〕=n1(CO2)消耗。a—b先发生2NaOH+CO2
BaCO3↓+H2O,可知n〔Ba(OH)2〕=n1(CO2)消耗。a—b先发生2NaOH+CO2![]() Na2CO3+H2O,后发生
Na2CO3+H2O,后发生![]() +CO2+H2O
+CO2+H2O![]() 2
2![]() ,到b点时相当于NaOH+CO2
,到b点时相当于NaOH+CO2![]() NaHCO3,因此n(NaOH)=n2(CO2)消耗,而n1(CO2)消耗=n2(CO2)消耗,
NaHCO3,因此n(NaOH)=n2(CO2)消耗,而n1(CO2)消耗=n2(CO2)消耗,
所以n〔Ba(OH)2〕=n(NaOH)。b—c发生的是BaCO3+CO2+H2O![]() Ba(HCO3)2,
Ba(HCO3)2,
所以n3(CO2)消耗=n(BaCO3)=n1(CO2)消耗=n〔Ba(OH)2〕。
答案:(1)Ba2++2OH-+CO2![]() BaCO3↓+H2O
BaCO3↓+H2O
(2)2OH-+CO2![]()
![]() +H2O, CO2+
+H2O, CO2+![]() +H2O
+H2O![]() 2
2![]()
(3)15
(4)1∶1

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目