题目内容
32g Cu与一定量的浓硫酸加热后,恰好完全反应,反应方程式如下:Cu+2H2SO4
CuSO4+SO2↑+2H2O
问:(1)得到SO2气体的体积(标准状况下)是多少?
(2)把所得的CuSO4 配制成250mL CuSO4溶液,所得溶液中溶质的物质的量浓度.
| ||
问:(1)得到SO2气体的体积(标准状况下)是多少?
(2)把所得的CuSO4 配制成250mL CuSO4溶液,所得溶液中溶质的物质的量浓度.
n(Cu)=
=0.5mol,
Cu+2H2SO4
CuSO4+SO2↑+2H2O
1mol 1mol 22.4L
0.5mol n(CuSO4) V(SO2)
(1)V(SO2)=
=11.2L
答:得到SO2气体的体积(标准状况下)是11.2L.
(2)n(CuSO4)=0.5mol
c(CuSO4)=
=2mol/L.
答:把所得的CuSO4 配制成250mL CuSO4溶液,所得溶液中溶质的物质的量浓度为2mol/L.
| 32g |
| 64g/mol |
Cu+2H2SO4
| ||
1mol 1mol 22.4L
0.5mol n(CuSO4) V(SO2)
(1)V(SO2)=
| 0.5mol×22.4L |
| 1mol |
答:得到SO2气体的体积(标准状况下)是11.2L.
(2)n(CuSO4)=0.5mol
c(CuSO4)=
| 0.5mol |
| 0.25L |
答:把所得的CuSO4 配制成250mL CuSO4溶液,所得溶液中溶质的物质的量浓度为2mol/L.

练习册系列答案
相关题目
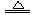 CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O