题目内容
下列有关对晶体的判断正确的是( )
| A、熔点MgO>NaCl>KCl |
| B、含有金属阳离子的晶体一定是离子晶体 |
| C、同主族元素形成的氧化物的晶体类型均相同 |
| D、沸点:H2O>PH3>NH3 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.根据影响离子晶体熔点的因素判断;
B.金属晶体含有金属离子;
C.碳族元素中,二氧化碳为分子晶体,二氧化硅为原子晶体;
D.氨气存在氢键,沸点较高.
B.金属晶体含有金属离子;
C.碳族元素中,二氧化碳为分子晶体,二氧化硅为原子晶体;
D.氨气存在氢键,沸点较高.
解答:
解:A.MgO中离子电荷数目为2,且离子半径最小,熔点最高,钠离子半径比钾离子半径小,NaCl熔点比KCl高,故A正确;
B.金属晶体含有金属离子,但为金属晶体,故B错误;
C.碳族元素中,二氧化碳为分子晶体,二氧化硅为原子晶体,故C错误;
D.氨气存在氢键,沸点较高,应为NH3>PH3,故D错误.
故选A.
B.金属晶体含有金属离子,但为金属晶体,故B错误;
C.碳族元素中,二氧化碳为分子晶体,二氧化硅为原子晶体,故C错误;
D.氨气存在氢键,沸点较高,应为NH3>PH3,故D错误.
故选A.
点评:本题考查晶体的类型和性质的判断,为高频考点,侧重于基本概念的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列物质属于不属于混合物的是( )
| A、纯碱 | B、石油 | C、煤 | D、碱石灰 |
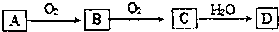

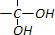
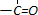
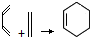
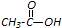
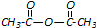
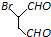 和
和 为原料合成
为原料合成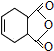 ,请设计合成路线(注明反应条件).
,请设计合成路线(注明反应条件).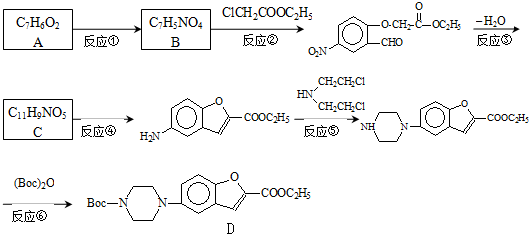
 ;
;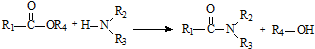 .
. 和
和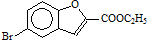 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式