题目内容
用质量分数为98%,密度为1.84g?mL-1的浓硫酸,配制240mL浓度为0.5mol?L-1的稀硫酸,其操作步骤如下:
A.用量筒量取一定体积的浓硫酸,缓缓注入约含50mL蒸馏水的烧杯里,并用玻璃棒搅拌.
B.用约30mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将每次洗涤液都注入容量瓶里.
C.将稀释后的硫酸小心地用玻璃棒引流入容量瓶.
D.继续向容量瓶中加蒸馏水,液面至刻度线下1cm~2cm.
E.盖紧瓶塞,反复上下颠倒,摇匀溶液.
F.用胶头滴管向容量瓶里逐滴滴入蒸馏水,至凹液面最低点恰好与刻度线相切.
据此填写:
(1)计算A步骤中量筒量取的浓硫酸体积为 mL
(2)正确的操作顺序是 .(填序号)
(3)除了玻璃棒、烧杯、量筒外,本操作还需用到的玻璃仪器有 .
(4)进行A步骤操作时,必须 后,才能进行后面的操作.
(5)如果在A步骤量取浓硫酸时,视线仰视,配制的稀硫酸的浓度将 .(填“偏高”、“偏低”或“无影响”).
A.用量筒量取一定体积的浓硫酸,缓缓注入约含50mL蒸馏水的烧杯里,并用玻璃棒搅拌.
B.用约30mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将每次洗涤液都注入容量瓶里.
C.将稀释后的硫酸小心地用玻璃棒引流入容量瓶.
D.继续向容量瓶中加蒸馏水,液面至刻度线下1cm~2cm.
E.盖紧瓶塞,反复上下颠倒,摇匀溶液.
F.用胶头滴管向容量瓶里逐滴滴入蒸馏水,至凹液面最低点恰好与刻度线相切.
据此填写:
(1)计算A步骤中量筒量取的浓硫酸体积为
(2)正确的操作顺序是
(3)除了玻璃棒、烧杯、量筒外,本操作还需用到的玻璃仪器有
(4)进行A步骤操作时,必须
(5)如果在A步骤量取浓硫酸时,视线仰视,配制的稀硫酸的浓度将
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)先计算出浓硫酸的物质的量浓度为c=
,然后根据溶液稀释定律C浓V浓=C稀V稀来计算; (2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(3)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(4)根据浓硫酸稀释时放热来分析;
(5)根据c=
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
| 1000ρω |
| M |
(3)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(4)根据浓硫酸稀释时放热来分析;
(5)根据c=
| n |
| V |
解答:
解:(1)浓硫酸的物质的量浓度为c=
=
=18.4mol/L,设需要的浓硫酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀可知:
250mL×0.5mol?L-1=18.4mol/L×VmL
解得V=6.8mL,故答案为:6.8;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:ACBDFE,故答案为:ACBDFE;
(3)操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.故所需仪器有量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管.故答案为:250mL容量瓶,胶头滴管;
(4)浓硫酸稀释时放热,故要将溶液冷却至室温再移液,故答案为:将溶液冷却至室温;
(5)量取浓硫酸时,视线仰视,会导致量取的浓硫酸的体积偏大,则配制的稀硫酸的浓度将偏高,故答案为:偏高.
| 1000ρω |
| M |
| 1000×1.84g/ml×98% |
| 98g/mol |
250mL×0.5mol?L-1=18.4mol/L×VmL
解得V=6.8mL,故答案为:6.8;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:ACBDFE,故答案为:ACBDFE;
(3)操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.故所需仪器有量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管.故答案为:250mL容量瓶,胶头滴管;
(4)浓硫酸稀释时放热,故要将溶液冷却至室温再移液,故答案为:将溶液冷却至室温;
(5)量取浓硫酸时,视线仰视,会导致量取的浓硫酸的体积偏大,则配制的稀硫酸的浓度将偏高,故答案为:偏高.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、物质的量浓度和体积都相同的盐酸和醋酸溶液,在与足量锌反应时,起始时二者产生H2速率基本相等 |
| B、100 mL 1 mol?L-1的盐酸和50 mL 2 mol?L-1的盐酸,分别与足量的锌反应时,两者放出H2速率和质量均相等 |
| C、100 mL pH=3的H2SO4和HCl溶液,与足量锌反应后,放出H2的质量相等 |
| D、100 mL pH=3的盐酸与醋酸溶液,与足量锌反应后,所得H2的质量相等 |
实验室可用如图来制取的气体是( )
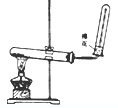

| A、氯气 | B、氧气 | C、氨气 | D、氢气 |
量取10mL碘的饱和水溶液,倒入分液漏斗中,然后注入4mL四氯化碳,用力振荡后静置,实验现象为( )
| A、液体分层,上层为四氯化碳层,黄色 |
| B、液体分层,上层为水层,紫色 |
| C、液体分层,下层为四氯化碳层,紫色 |
| D、液体分层,下层为水层,黄色 |
下列有关实验操作和说法正确的是( )
| A、用pH试纸检验气体的酸碱性时,一定要先用蒸馏水润湿 |
| B、润洗滴定管:从滴定管上口加入所要盛装的酸或碱溶液至“0”刻线,再将液体从滴定管下部放出,重复操作2~3次 |
| C、用瓷坩埚加热熔化碳酸钠固体 |
| D、Mg和Al分别为电极,插入NaOH溶液中,构成原电池,探究Mg、Al的活泼性 |
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2→CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:分析实验数据所得出的结论不正确的是( )
| 实验 序号 | 初始浓度c/mol?L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.001 0 | 290 |
| ② | 1.60 | 0.20 | 0.001 0 | 145 |
| ③ | 0.80 | 0.40 | 0.001 0 | 145 |
| ④ | 0.80 | 0.20 | 0.002 0 | 580 |
| A、增大c(CH3COCH3),v(Br2)增大 |
| B、实验②和③的v(Br2)相等 |
| C、增大c(HCl),v(Br2)增大 |
| D、增大c(Br2),v(Br2)增大 |