题目内容
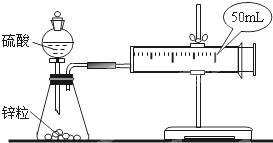 两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间.
两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间.(1)当收集到10mL H2时,哪个实验所耗时间较长?为什么?
(2)活塞外移的情况是
A.均匀外移B.先快后慢C.先慢后快D.先慢后快然后又逐渐减慢
你选择的理由是
考点:探究影响化学反应速率的因素
专题:化学反应速率专题
分析:(1)根据物质的量浓度对反应速率的影响进行分析反应速率大小,根据t=
判断反应时间;
(2)锌与稀硫酸的反应为放热反应,开始时温度对反应速率影响较大,之后氢离子浓度减小,则浓度对反应速率影响为主.
| n |
| v |
(2)锌与稀硫酸的反应为放热反应,开始时温度对反应速率影响较大,之后氢离子浓度减小,则浓度对反应速率影响为主.
解答:
解:(1)由于浓度越大,反应速率越快,则4mol/L的硫酸与锌反应的速率反应1mol/L的硫酸,则收集10mL氢气是,1mol/L的硫酸需要的时间长,
故答案为:1mol/L的硫酸的时间长,因为浓度小的反应速度慢;
(2)由于该反应是放热反应,温度升高,反应速度加快,开始时温度对反应速率影响较大,之后随反应的进行,H+浓度不断减小,浓度对反应速率影响较大,则反应速度减慢,所以D正确,
故答案为:D;此反应是放热反应,温度升高,反应速度加快,随反应的进行,H+浓度不断减小,反应速度减慢.
故答案为:1mol/L的硫酸的时间长,因为浓度小的反应速度慢;
(2)由于该反应是放热反应,温度升高,反应速度加快,开始时温度对反应速率影响较大,之后随反应的进行,H+浓度不断减小,浓度对反应速率影响较大,则反应速度减慢,所以D正确,
故答案为:D;此反应是放热反应,温度升高,反应速度加快,随反应的进行,H+浓度不断减小,反应速度减慢.
点评:本题考查了探究影响化学反应速率达到因素,题目难度不大,试题侧重基础知识的考查,注意掌握温度、浓度等因素对化学反应速率的影响,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
实验室用固态不纯氯化钠(含少量泥沙和Na2SO4杂质)制取纯净氯化钠溶液.下列操作可供选用:①逐滴加入稀盐酸至稍过量;②煮沸;③加蒸馏水溶解;④过滤 ⑤加入稍过量的Na2CO3溶液;⑥加入稍过量的BaCl2溶液.上述实验操作的正确顺序应是( )
| A、①②③④⑤⑥ |
| B、④③⑥⑤①② |
| C、③⑥⑤④①② |
| D、③⑥⑤①④② |
下列说法正确的是( )
| A、糖类、油脂和蛋白质是基本营养物质 |
| B、蛋白质水解的最终产物是多肽 |
| C、糖尿病人不能食用含糖和淀粉的食品 |
| D、向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
关于3Cl2+6KOH
KClO3+5KCl+3H2O反应,以下说法错误的是( )
| ||
| A、Cl2既是氧化剂,又是还原剂 |
| B、3 mol氯气参加反应转移5 mol电子 |
| C、氧化产物的物质的量是还原产物的物质的量的5倍 |
| D、每有1 mol原子被氧化的同时就有5 mol原子被还原 |
已知:HCl(aq)与NaOH(aq)反应的△H=-55.6kJ/mol; HCN(aq)与NaOH(aq)反应的△H=-12.1kJ/mol.则HCN在水溶液中电离的△H等于( )
| A、+43.5 kJ/mol |
| B、-67.7 kJ/mol |
| C、+67.7 kJ/mol |
| D、-43.5 kJ/mol |
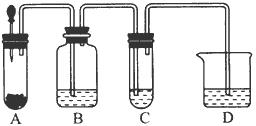 小明在阅读《化学课外补充材料(高一)》时,注意到该书中的下列描述:浓盐酸和次氯酸钙能发生反应并产生氯气,反应为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.小明设计了如图的装置验证上述反应原理.(已知:胶头滴管中装浓盐酸)
小明在阅读《化学课外补充材料(高一)》时,注意到该书中的下列描述:浓盐酸和次氯酸钙能发生反应并产生氯气,反应为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.小明设计了如图的装置验证上述反应原理.(已知:胶头滴管中装浓盐酸)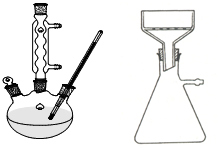 某实验室制取苯甲酸的过程如下:
某实验室制取苯甲酸的过程如下: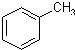 +2KMnO4
+2KMnO4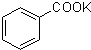 +MnO2+KOH+H2O
+MnO2+KOH+H2O