题目内容
11. (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa、25℃时,16gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ.N2H4完全燃烧反应的热化学方程式是N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol.
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa、25℃时,16gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ.N2H4完全燃烧反应的热化学方程式是N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol.(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼--空气燃料电池放电时:正极的电极反应式是2H2O+O2+4e-=4OH-;负极的电极反应式是N2H4+4OH--4e-=4H2O+N2↑.
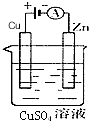
(3)如图是一个电化学过程示意图.
①锌片上发生的电极反应方程式是Cu2++2e-=Cu.
②假设使用肼--空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼--空气燃料电池理论上消耗标准状况下的空气112L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是ClO-+2NH3=N2H4+Cl-+H2O.
(5)将0.3molAgNO3、0.4molCu(NO3)2和0.1molKCl溶于水配成100ml溶液,用惰性电极电解一段时间后,当阴极生成0.1mol气体时,此时,另一极上的气体体积(标准状况)为6.72L.
分析 (1)根据肼和反应热的关系计算出其燃烧热,并写出其相应的热化学方程式;
(2)燃料电池中,负极上投放的是燃料,负极上燃料失电子发生氧化反应;
(3)①电解池的阴极上是阳离子发生得电子的还原反应;
②根据电极反应,结合电子守恒和空气的组成情况来回答;
(4)NaClO氧化NH3可以制得肼,还生成氯化钠;
(5)将0.3mol AgNO3、0.4mol Cu(NO3)2和0.1mol KCl溶于水,会发生反应生成氯化银沉淀,电解混合溶液时,阴极发生Ag++e-=Ag,Cu2++2e-=Cu,然后是氢离子放电:2H++2e-=H2↑,结合两极转移电子数目相等和电极方程式计算.
解答 解:(1)16gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ,32g肼的物质的量为1mol,1molN2H4在氧气中完全燃烧生成氮气放出热量624kJ,所以其热化学反应方程式为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol,
故答案为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol;
(2)燃料电池中,负极上投放的是燃料,负极上燃料失电子发生氧化反应,在碱性环境下的反应式为:N2H4+4OH--4e-=4H2O+N2↑,正极上是氧气发生得电子的还原反应,在碱性环境下,电极反应式为:2H2O+O2+4e-=4OH-,
故答案为:2H2O+O2+4e-=4OH-;N2H4+4OH--4e-=4H2O+N2↑;
(3)①与电源负极相连的是电解池的阴极,在阴极上阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu,
故答案为:Cu2++2e-=Cu;
②铜片上的电极反应为:Cu-2e-=Cu,Cu的质量变化128g,根据电极反应,转移电子为4mol,根据反应N2H4+O2=N2+2H2O,当转移电子4mol时,消耗氧气的物质的量是1mol,氧气的体积是空气体积的五分之一,所以消耗空气的体积是5mol,即112L,
故答案为:112;
(4)NaClO氧化NH3可以制得肼的离子方程式为:ClO-+2NH3=N2H4+Cl-+H2O,
故答案为:ClO-+2NH3=N2H4+Cl-+H2O;
(5)将0.3mol AgNO3、0.4mol Cu(NO3)2和0.1mol KCl溶于水,会发生反应生成氯化银沉淀,溶液中的离子有银离子0.2mol,铜离子0.4mol,其余是钾离子和硝酸根离子,阴极发生的还原反应有:Ag++e-=Ag,Cu2++2e-=Cu,银离子0.2mol得电子0.2mol,铜离子0.4mol得电子0.8mol,然后是氢离子放电:2H++2e-=H2↑,阴极生成0.1mol气体时得到电子0.2mol,可知阴极共得到1.2mol电子,阳极发生:4OH--4e-=O2↑+2H2O,转移电子1.2mol时,生成氧气0.3mol,气体体积=0.3mol×22.4L/mol=6.72L,
故答案为:6.72L.
点评 本题是一道有关热化学和电化学知识的综合考察知识题目,要求学生具有分析和解决问题的能力,第(5)题易错,注意溶液中离子的成分和放电顺序.

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案| A. | 氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 | |
| B. | SO2溶于水,其水溶液能导电,说明SO2是电解质 | |
| C. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度从而增大与氢氧化溶液的接触面积,从而加快油脂皂化反应速率 | |
| D. | 某溶液用硝酸酸化无现象,再滴加氯化钡溶液有白色沉淀产生,说明溶液中有SO42- |
| A. | CO的还原性强于Pd | |
| B. | 反应中PdCl2被氧化 | |
| C. | 若反应生成22.4 L CO2,则转移电子的物质的量一定为2 mol | |
| D. | CO气体只有在高温下才能表现出还原性 |
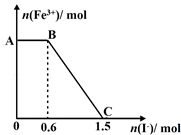 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+,现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+,现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A. | 图中AB段的氧化剂为K2Cr2O7 | |
| B. | 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 | |
| C. | 开始加入的K2Cr2O7为0.25 mol | |
| D. | 共有1molFeSO4被氧化 |
| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 电解熔融氧化铝:2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑ | |
| C. | NaHCO3溶液与稀H2SO4反应:HCO3-+H+═H2O+CO2↑ | |
| D. | 向Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
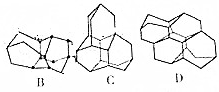
 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.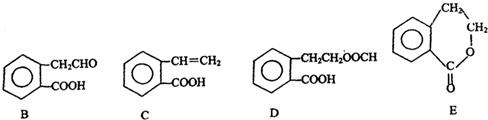
 .
. .
.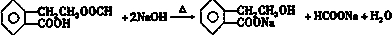 .
.